题目内容
(12分)(1)氮元素基态原子核外未成对电子数为 个;
(2)C、N、O三种元素第一电离能从大到小的顺序是_____________;
(3)某晶体的晶胞如图所示,X位于体心,Y位于4个面心,Z位于8个顶点,该晶体中 X、Y、Z的粒子个数比为______________;

(4)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态
电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
(5)某化合物其组成可用CoCl3·5NH3表示。把CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的化学式(钴的配位数为6)_____________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是_____________;
(3)某晶体的晶胞如图所示,X位于体心,Y位于4个面心,Z位于8个顶点,该晶体中 X、Y、Z的粒子个数比为______________;

(4)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态
电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
(5)某化合物其组成可用CoCl3·5NH3表示。把CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的化学式(钴的配位数为6)_____________________。
(12分,每空2分)(1)3 (2分)
(2)N、O 、C (2分) (3)1∶2∶1 (2分)
(4)1s22s22p63s23p63d10或[Ar] 3d10 (2分) sp2、sp3(2分)
(5)[Co(NH3)5Cl]Cl2 (2分)
(2)N、O 、C (2分) (3)1∶2∶1 (2分)
(4)1s22s22p63s23p63d10或[Ar] 3d10 (2分) sp2、sp3(2分)
(5)[Co(NH3)5Cl]Cl2 (2分)
(1)根据构造原理可知,氮元素基态原子核外电子排布式为11s22s22p3,所以未成对电子数为3个。
(2)非金属性越强,第一电离能越大,但由于氮原子的2p轨道是半充满状态,稳定性强,所以氮元素的第一电离能大于氧元素的,即顺序是N>O>C 。
(3)X位于体心,Y位于4个面心,Z位于8个顶点,所以该晶胞中含有的X、Y、Z原子数分别是1、4×1/2=2、8×1/8=1,因此晶体中 X、Y、Z的粒子个数比为1∶2∶1。
(4)根据构造原理可知Zn2+基态电子排布式为1s22s22p63s23p63d10或[Ar] 3d10。分子中5个饱和碳原子全部形成单键,所以是sp3杂化。而羧基中的碳原子含有碳养双键,所以是sp2杂化。
(5)1 mol CoCl3·5NH3只生成2 mol AgCl,说明作为配体的氯离子只有1个,所以配合物结构的化学式[Co(NH3)5Cl]Cl2 。
(2)非金属性越强,第一电离能越大,但由于氮原子的2p轨道是半充满状态,稳定性强,所以氮元素的第一电离能大于氧元素的,即顺序是N>O>C 。
(3)X位于体心,Y位于4个面心,Z位于8个顶点,所以该晶胞中含有的X、Y、Z原子数分别是1、4×1/2=2、8×1/8=1,因此晶体中 X、Y、Z的粒子个数比为1∶2∶1。
(4)根据构造原理可知Zn2+基态电子排布式为1s22s22p63s23p63d10或[Ar] 3d10。分子中5个饱和碳原子全部形成单键,所以是sp3杂化。而羧基中的碳原子含有碳养双键,所以是sp2杂化。
(5)1 mol CoCl3·5NH3只生成2 mol AgCl,说明作为配体的氯离子只有1个,所以配合物结构的化学式[Co(NH3)5Cl]Cl2 。

练习册系列答案
相关题目
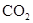 转化为具有类似
转化为具有类似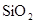 结构的原子晶体,下列关于
结构的原子晶体,下列关于 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8
)中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8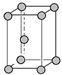 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12
中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12