题目内容
LED照明是我国制造业为人类做出的一大贡献。目前市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如下图。试回答:
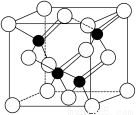
(1)镓的基态原子的电子排布式是__________。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为__________,与同一个镓原子相连的砷原子构成的空间构型为__________。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是__________。(用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为__________。
(5)比较二者的第一电离能:As__________Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是__________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.GaP与GaAs互为等电子体
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
(1)1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)
(2)4 正四面体 (3)NH3>AsH3>PH3 (4)sp2 (5)> (6)BCD
【解析】(1)镓是31号元素,电子排布式为1s22s22p63s23p63d104s24p1。(2)砷化镓晶胞中砷原子8个在立方体顶角,6个在面上,该晶胞所包含砷原子数为8×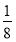 +6×
+6×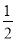 =4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。
=4,而镓原子周围是4个均匀分布的砷原子为正四面体型。(3)NH3分子间有氢键沸点最高,其它分子按分子量大小排列,NH3>AsH3>PH3。(4)镓原子与3个甲基结合,且镓的价电子都成键,所以为sp2杂化。(5)砷的非金属性强,第一电离能大。(6)砷化镓晶胞与NaCl不同,A项错误。GaP与GaAs原子个数比相同,但电子总数不同,B项错误。As非金属性强,电负性也强,C正确。镓有3个价电子,但形成4个共价键,说明有一个配位键。D正确。

 名校课堂系列答案
名校课堂系列答案分析下表中各项的排布规律,按此规律排布第26项应为( )
1 | 2 | 3 | 4 | 5 |
C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 |
6 | 7 | 8 | 9 | 10 |
C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O