题目内容
下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是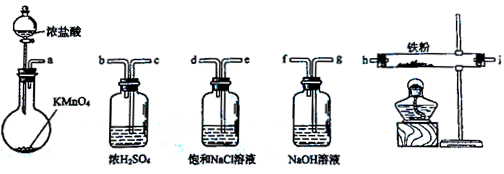
| A.a-b-c-d-e-e-f-g-h |
| B.a-e-d-c-b-h-i-g |
| C.a-d-e-c-b-h-i-g |
| D.a-c-b-d-e-h-i-f |
B
解析

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
碘元素有“智力元素”之称。研究性学习小组做了如下实验探究海带中碘元素存在并测定其中碘元素的含量。
(1)操作I为灼烧,则灼烧时用____盛装海带,操作II为____________________________;
(2)水浸时通常要将悬浊液煮沸2~3min,目的是______________________________;
(3)操作III,是同学们对溶液A中碘元素的存在形式进行的探究实验。
[推测]:①以IO3ˉ形式存在; ②以Iˉ形式存在
[查阅资料]:IO3ˉ具有较强的氧化性,I2+2S2O32ˉ=2Iˉ+S4O62ˉ
将上述溶液稀释配制成200mL溶液,请完成下列实验探究。限选试剂:3%H2O2溶液、KSCN溶液、FeCl2溶液、稀硫酸。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管I、II | 无现象 | |
| ② | 往试管I中加入______ | 无现象 | 证明不是以IO3ˉ形式存在 |
| ③ | 往试管II中加入_______ | _______________ | 证明以 形式存在 形式存在 |
(4)定量检验海带中的碘含量:
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将Iˉ氧化为I2并得到溶液B;
②在溶液B加入两滴淀粉溶液,用0.01mol/LNa2S2O3溶液,滴定至终点,终点现象为___________,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,计算海带中碘元素的百分含量_________________.(假设操作I、II过程中碘不损失,相对原子量I-127)
用下图所示的装置制取、提纯并收集表中的四种气体,图中a、b、c表示相应仪器加入的试剂,未考虑尾气处理的问题,其中可行的是
| | 气体 | a | b | C |
| A |  | 浓氨水 | 生石灰 | 碱石灰 |
| B |  | 稀硝酸 | 铜片 | 碱石灰 |
| C |  | 浓硫酸 | 浓盐酸 | 氯化钙 |
| D | SO2 | 浓硫酸 | 铜片 | 硅胶 |
利用下列实验装置进行的相应实验,能达到实验目的的是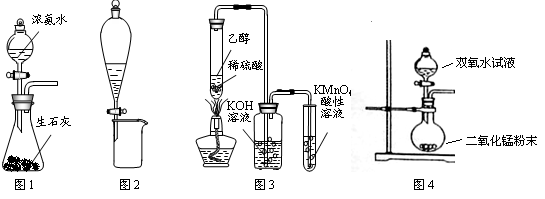
| A.图1所示装置可制备氨气 |
| B.图2所示装置可分离CH3CH2OH和CH3COOC2H5的混合液 |
| C.图3所示装置可制备、收集乙烯并验证其易被氧化 |
| D.图4所示装置可制备氧气 |
如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是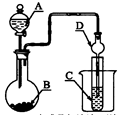
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色 |
| B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 |
| C.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色 |
| D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀 |
下列实验设计方法正确的是
| A.向卤代烃加硝酸酸化的硝酸银来检验其中的卤族素元素 |
| B.实验用NH4Cl固体受热分解来制备NH3 |
| C.用盐酸和澄清石灰水来检验某物质是否含有CO32- |
| D.可用下图所示的装置和药品来研究反应物浓度对反应速率的影响 |
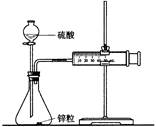
下列气体组(括号内为杂质)可用如图装置提纯的是( )
| A.H2S(HCl) | B.NO2(CO2) | C.C2H6(C2H4) | D.CO2(H2S) |
用如图装置制取少量某无色非金属氧化物气体,则锥形瓶X内的药品应是( )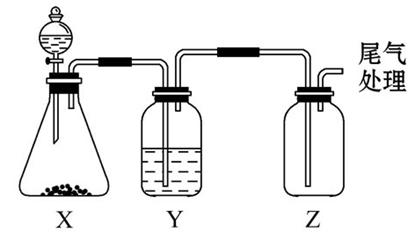
| A.铜和稀硝酸 | B.铜和浓硝酸 |
| C.碳酸钙与稀硫酸 | D.亚硫酸钠和浓硫酸 |
下列有关实验原理或实验操作正确的是( )
| A.用(a)装置制备并收集少量NO2气体 |
| B.通过(b)装置实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
| C.装置(c)可用于定量测定H2O2的分解速率 |
| D.装置(d)可用于实验室制取乙酸乙酯 |