题目内容
在氧气中充分燃烧1克含杂质的硫铁矿试样,得到残余固体0.76克(假设杂质不参加反应),问生产10吨98%的浓硫酸需要这种矿石多少吨?(反应过程中硫损失2%)
需该矿石8.5吨。
|
480克 320克 160克
1克×X 1克-0.76克=0.24克
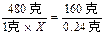
X=72%

 FeS2 2H2SO4
FeS2 2H2SO4120 196
Y·72%×(1-2%) 10吨×98%
Y=8.5吨

练习册系列答案
相关题目
题目内容
|
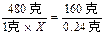

 FeS2 2H2SO4
FeS2 2H2SO4