题目内容
根据下图所示的装置进行相关实验,对实验现象预测正确的是( )
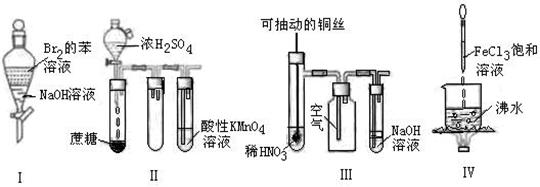

| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色不会褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
D
单质溴能和氢氧化钠反应,所以溶液褪色,A不正确。浓硫酸具有脱水性和强氧化性,在反应中能产生SO2,SO2具有还原性,能使酸性高锰酸钾溶液褪色,B不正确。铜和稀硝酸反应生成NO。NO极易被氧化生成红棕色NO2气体,C不正确,所以正确的答案选D。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目