题目内容
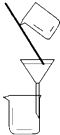
【题目】50mL 0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算反应热. 
(1)烧杯间填满泡沫塑料的作用是;
(2)如图所示,仪器A的名称是;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H﹣57.3KJ/mol(填“>”、“<”或“=”);
(3)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出稀硝酸和稀氢氧化钾溶液反应的中和热的热化学方式;
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)
(5)为了测量某酸碱反应的中和热,计算时至少需要的数据是
①酸的浓度和体积 ②碱的浓度和体积 ③比热容 ④反应后溶液的质量 ⑤生成水的物质的量 ⑥反应前后温度变化⑦操作所需的时间
A.①②③④
B.①③④⑤
C.③④⑤⑥
D.全部.
【答案】
(1)减少实验过程中的热量损失
(2)环形玻璃搅拌棒;>
(3)HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)△H=﹣57.3KJ/mol
(4)偏小
(5)C
【解析】解:(1)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失;
所以答案是:减少实验过程中的热量损失;(2)由装置图可知,仪器A的名称是环形玻璃搅拌棒;中和反应是放热反应,温度计上的酸与NaOH溶液反应放热,使温度计读数升高,温度差偏小,热量偏小,但测得的中和热偏大,即△H>﹣57.3KJ/mol;
所以答案是:环形玻璃搅拌棒;>;(3)稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,稀硝酸和稀氢氧化钾溶液都是强酸和强碱的稀溶液,则反应的热化学方程式为:HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)△H=﹣57.3KJ/mol;
所以答案是:HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)△H=﹣57.3KJ/mol;(4)一水合氨为弱碱,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量小于57.3kJ;
所以答案是:偏小;(5)由反应热的计算公式△H=﹣ ![]() 可知,酸碱反应的中和热计算时,至少需要的数据有:比热容c,酸的浓度和体积、碱的浓度和体积,反应前后温度变化△T,然后计算出反应后溶液的质量、生成水的物质的量;
可知,酸碱反应的中和热计算时,至少需要的数据有:比热容c,酸的浓度和体积、碱的浓度和体积,反应前后温度变化△T,然后计算出反应后溶液的质量、生成水的物质的量;
故选:C.

 阅读快车系列答案
阅读快车系列答案【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般采用下列反应合成甲醇:
CO(g)+2H2(g)═CH3OH(g)△H1
①下表所列数据是反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断△H10 (填“>”、“=”或“<”).
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为(从上表中选择).