题目内容
7.下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是( )| A. | a原子的最外层电子数比B原子的最外层电子数少 | |
| B. | a原子电子层数比b原子的电子层数多 | |
| C. | 1mol a 从酸中置换H+生成的H2比1 mol b从酸中置换H+生成的H2多 | |
| D. | 常温时,a能从水中置换出氢,而b不能 |
分析 金属的金属性越强,其最高价氧化物的水化物碱性越强,其单质的还原性较强,与酸或水反应剧烈程度越大,据此分析解答.
解答 解:金属的金属性越强,其最高价氧化物的水化物碱性越强,其单质的还原性较强,与酸或水反应剧烈程度越大,
A.金属的金属性强弱与最外层电子数多少无关,如:最外层电子数Al>Mg,但活泼性Mg>Al,故A错误;
B.金属的金属性强弱与电子层数无关,如Fe的电子层数大于Na,但活泼性Na>Fe,故B错误;
C.金属的金属性强弱与失电子多少无关,如相同物质的量的Al和Mg分别与酸反应,铝得到氢气比镁多,但活泼性Mg>Al,故C错误;
D.常温下,a能从水中置换出氢,而b不能,说明活泼性a>b,故D正确;
故选D.
点评 本题考查金属活泼性强弱判断,侧重考查学生分析判断能力,注意金属性活泼性强弱与失电子难易程度有关,与失电子多少、最外层电子数、电子层数等都无关,为易错题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.中国科技大学的科学家将C60分子组装在一单层分子膜表面,在-268℃时冻结分子的热振荡,利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图象.下列化合物分子中一定既含σ键又含π键的是( )
| A. | N2 | B. | CO2 | C. | C2H6O | D. | H2O2 |
18.氢元素与其它元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )
| A. | 一个D2O分子所含的中子数为8 | |
| B. | NH3的结构式为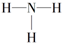 | |
| C. | HCl的电子式为H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$]- | |
| D. | 热稳定性:HCl>HF |
15.下列物质中,不属于羧酸类的是( )
| A. | 草酸 | B. | 苯甲酸 | C. | 亚油酸 | D. | 石炭酸 |
2.利用下列反应不能制得括号中纯净物质的是( )
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 等物质的量的氯气与乙烷在光照下反应(氯乙烷) | |
| C. | 乙烯与水加成(乙醇) | |
| D. | 乙烯与氯化氢在一定条件下反应(氯乙烯) |
12.下列说法正确的是( )
| A. | 同一原子中,2p、3p、4p能级的轨道数依次增多 | |
| B. | 电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则 | |
| C. | 共价键都有方向性 | |
| D. | 正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族 |
19.下列原子或离子的基态电子排布式正确的是( )
| A. | Ni2+:[Ar]3d8 | B. | Cu:[Ar]3d94s2 | C. | S2-:[Ne]2s23p6 | D. | Si:[Ar]3s23p2 |
16.下列有关化学键的说法中,不正确的是( )
| A. | 氢键不是化学键,而是一种特殊的分子间作用力 | |
| B. | 化学键可以使离子相结合,也可以使原子相结合 | |
| C. | 化学反应过程中,反应物分子的化学键断裂消耗能量,生成物分子中化学键形成放出能量 | |
| D. | 氯化钠中存在离子键,所以食盐水是离子化合物 |
 ;
;