题目内容
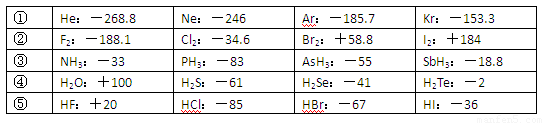
已知一些单质、化合物的沸点(1.01×105Pa,单位:℃)如下表所示:
结合上表有关信息回答下列问题:
(1)判断下列说法不正确的是 (填“序号”).
A.同周期元素的氢化物,原子序数越大,沸点越高
B.上表中H2O、HF中由于含有氢键,故其分子特别稳定
C.上表中,多数物质的沸点均与相对分子质量存在一定的关系
D.周期表中各主族元素的单质其沸点都随原子序数的增大而升高
E.氢化物的稳定性越高,其沸点越高
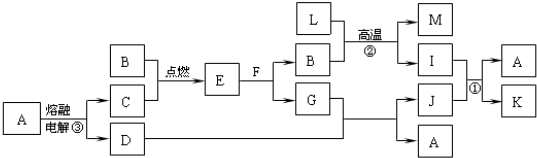
(2)写出②系列中物质主要化学性质的递变规律(任写一种): ;能说明该递变规律的化学事实是 (任写一例,用离子方程式表示).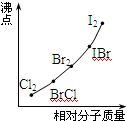
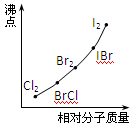
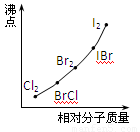
(3)部分XX′型卤素互化物(X、X′表示不同的卤原子)和卤素单质的沸点也与其相对分子质量存在着如图所示的关系.试推测ICl的沸点所处的最小范围 (填“物质的化学式”).
| ① | He:-268.8 | Ne:-246 | Ar:-185.7 | Kr:-153.3 |
| ② | F2:-188.1 | Cl2:-34.6 | Br2:+58.8 | I2:+184 |
| ③ | NH3:-33 | PH3:-83 | AsH3:-55 | SbH3:-18.8 |
| ④ | H2O:+100 | H2S:-61 | H2Se:-41 | H2Te:-2 |
| ⑤ | HF:+20 | HCl:-85 | HBr:-67 | HI:-36 |
(1)判断下列说法不正确的是
A.同周期元素的氢化物,原子序数越大,沸点越高
B.上表中H2O、HF中由于含有氢键,故其分子特别稳定
C.上表中,多数物质的沸点均与相对分子质量存在一定的关系
D.周期表中各主族元素的单质其沸点都随原子序数的增大而升高
E.氢化物的稳定性越高,其沸点越高
(2)写出②系列中物质主要化学性质的递变规律(任写一种):

(3)部分XX′型卤素互化物(X、X′表示不同的卤原子)和卤素单质的沸点也与其相对分子质量存在着如图所示的关系.试推测ICl的沸点所处的最小范围
分析:(1)从表中得出一些信息,同一族稀有气体、非金属单质、氢化物的沸点数据变化规律,同时注意由于氢键的存在,沸点变化的特殊性,以及金属单质与非金属单质的不同;
(2)同族元素的单质随原子序数的递增,单质性质出现递变性;
(3)从图中可看出组成和结构相似的物质,相对分子质量越大,沸点越高,根据沸点和相对分子质量的关系来判断.
(2)同族元素的单质随原子序数的递增,单质性质出现递变性;
(3)从图中可看出组成和结构相似的物质,相对分子质量越大,沸点越高,根据沸点和相对分子质量的关系来判断.
解答:解:(1)A.对不含氢键的氢化物来说,同周期元素的氢化物,原子序数越大,沸点越高,若含氢键,则比分子量的要高,故A错误;
B.氢键的存在,使熔沸点升高,与化学性质无关,故B错误;
C.从表中数据看,除了水、氨气、氢氟酸外,其他都和相对分子质量存在关系,故C正确;
D.金属单质随相对原子质量的增大,沸点降低,故D错误;
E.氢化物的稳定性和化学键的强弱有关,与沸点无关,故E错误;
故选:ABDE;
(2)卤素单质随原子序数的递增,性质存在递变性,如氧化性逐渐减弱,与氢化合的难易程度由易到难等,卤素单质间的置换反应能证明这一点.
故答案为:单质的氧化性逐渐减弱;Cl2+2Br-═2Cl-+Br2;
(3)从图中可看出,组成和结构相似的物质,相对分子质量越大,沸点越高,由于ICl的相对分子质量介于Br2和IBr沸点之间,所以沸点也介于Br2的沸点和IBr沸点之间,
故答案为:介于Br2的沸点和IBr沸点之间.
B.氢键的存在,使熔沸点升高,与化学性质无关,故B错误;
C.从表中数据看,除了水、氨气、氢氟酸外,其他都和相对分子质量存在关系,故C正确;
D.金属单质随相对原子质量的增大,沸点降低,故D错误;
E.氢化物的稳定性和化学键的强弱有关,与沸点无关,故E错误;
故选:ABDE;
(2)卤素单质随原子序数的递增,性质存在递变性,如氧化性逐渐减弱,与氢化合的难易程度由易到难等,卤素单质间的置换反应能证明这一点.
故答案为:单质的氧化性逐渐减弱;Cl2+2Br-═2Cl-+Br2;
(3)从图中可看出,组成和结构相似的物质,相对分子质量越大,沸点越高,由于ICl的相对分子质量介于Br2和IBr沸点之间,所以沸点也介于Br2的沸点和IBr沸点之间,
故答案为:介于Br2的沸点和IBr沸点之间.
点评:本题考查了元素周期律的应用,注意元素性质存在递变性,也有特殊性,如氢键的存在,使沸点升高等,特别注意,氢键只影响物理性质,与物质的稳定性无关.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(10分)已知一些单质、化合物的沸点(1.01×105Pa,单位:℃)如下表所示: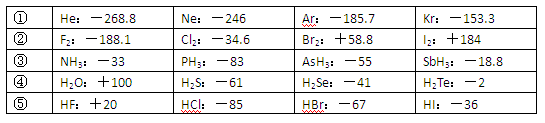
结合上表有关信息回答下列问题:
(1)判断下列说法不正确的是
| A.同周期元素的氢化物,原子序数越大,沸点越高 |
| B.上表中H2O、HF中由于含有氢键,故其分子特别稳定 |
| C.上表中,多数物质的沸点均与相对分子质量存在一定的关系 |
| D.周期表中各主族元素的单质其沸点都随原子序数的增大而升高 |
(2)写出②系列中物质主要化学性质的递变规律(任写一种): ;能说明该递变规律的化学事实是 (任写一例,用离子方程式表示)。
(3)除极少数情况,同一系列中物质的沸点与相对分子质量之间存在一定的关系,该关系是 。
(4)部分XX’型卤素互化物(X、X’表示不同的卤原子)和卤素单质的沸点也与其相对分子质量存在着如右图所示的关系。试推测ICl的沸点所处的最小范围 (填“物质的化学式”)。