题目内容
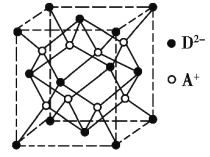
【题目】A、B、C、D、X、Y 为元素周期表中六种主族元素,其原子序数依次增大,均小于54;常温下 A2B呈液态;高纯 C单质是良好的半导体材料; D、X、Y 原子最外层电子数均为 7;过渡元素 Z与 B可形成多种化合物,其中红棕色粉末 Z2B3常用作红色油漆和涂料。
请按要求回答下列问题:
(1)将D2的水溶液加入浅绿色的 ZD2溶液中发生反应的离子方程式为______________。
(2)学生甲认为 X2和 Y2都可能将 Z2+氧化为 Z3+,他推理的依据是_______________。
(3)学生乙认为 X2能将 Z2+氧化为 Z3+,但 Y2不能。学生乙推理的依据是____________。
(4)A与 B可形成既含极性键又含非极性键的化合物 W。 W 的水溶液呈弱酸性,常用作无污染的消毒杀菌剂等。
①W 的电子式为___________,W 的第一步电离方程式为____________。
②如果配制 W 溶液的水中含有 Z3+,会削弱 W 的消毒杀菌能力,甚至会完全失去杀菌作用。试用化学方程式表示其原因:________________。
(5)铅(Pb)、锡(Sn)、锗(Ge)与元素 C 同主族;常温下其单质在空气中,锡、锗不反应,而铅表面会生成一层氧化铅;锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为___________;
②它们+4 价氢氧化物的碱性由强到弱的顺序为_______________(填化学式)。
【答案】(1)2Fe2++Cl2=2Fe3++2Cl-(2分);
(2)Br、I与Cl均为ⅦA族元素,其单质具有较强的氧化性(2分)
(3)Br、I与Cl均为ⅦA族元素,从上到下卤素单质氧化性逐渐减弱(2分);
(4)①![]() (2分)H2O2
(2分)H2O2![]() H++HO2(2分)②2H2O2
H++HO2(2分)②2H2O2![]() 2H2O+O2↑(2分)
2H2O+O2↑(2分)
(5)①32(1分)②Pb(OH)4>Sn(OH)4>Ge(OH)4(1分)
【解析】试题分析:六种主族元素A、B、C、D、X、Y,其原子序数依次增大,均小于54;常温下A2B呈液态,A2B是H2O,故A为氢元素,B为氧元素;高纯C单质具有良好的半导体性能,C为Si元素;D、X、Y原子核外最外层电子数均为7,处于第ⅦA族,且Y的原子序数小于54,故D为Cl元素、X为Br元素、Y为I元素;过渡元素Z与B可形成多种化合物,其中红棕色粉末Z2B3常用作外墙涂料,Z为Fe元素,则
(1)将Cl2水溶液滴入浅绿色的FeCl2溶液中发生反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-;
(2)Cl、Br、I均是第ⅦA族元素,其单质的氧化性均较强,因此X2和Y2都可能将Z2+氧化为Z3+;
(3)由于Cl、Br、I均是第ⅦA族元素,自上而下非金属性减弱,其单质的氧化性减弱,所以学生乙认为X2和Y2都不能将Z2+氧化为Z3+;
(4)A与B可形成既含极性键又含非极性键的化合物W,W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等,W为H2O2,①H2O2中氢原子与氧原子之间形成一对共用电子对,氧原子之间形成1对共用电子对,故电子式为![]() ,其水溶液呈弱酸性,为弱电解质,电离出H+、HO2-,故W第一步电离方程式为H2O2
,其水溶液呈弱酸性,为弱电解质,电离出H+、HO2-,故W第一步电离方程式为H2O2![]() H++HO2;
H++HO2;
②如果配制W溶液的水中含有Fe3+,Fe3+对H2O2的分解其催化剂作用,发生反应2H2O2![]() 2H2O+O2↑。
2H2O+O2↑。
(5)①锗再硅元素的下一周期,二者原子序数形成18,故锗的原子序数为14+18=32;②同主族自上而下金属性增强,金属性越强,它们+4价氢氧化物的碱性越强,故碱性由强到弱顺序为Pb(OH)4>Sn(OH)4>Ge(OH)4。