题目内容

有关氢氧化物沉淀的pH见下表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
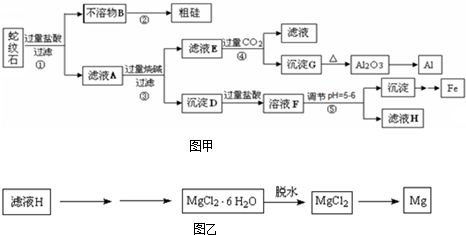
(2)操作④中滤液E与过量CO2反应生成沉淀G的离子方程式为:
(3)操作⑤中调节pH到5~6时,可以用到的试剂(填序号)
a. NaOH溶液 b.氨水 c. Fe2O3 d. Mg(OH)2
(4)从滤液H制取金属Mg的流程如下:
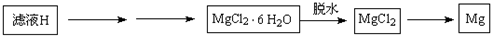
Ⅰ.流程中由滤液H中得到MgCl2?6H2O的方法是
Ⅱ.在干燥的HCl气流中加热MgCl2?6H2O制取无水氯化镁的原因是
Ⅲ.冶炼镁的方法用化学方程式表示为
| ||
| 熔融 |
| ||
| 熔融 |
(2)滤液A中含有镁离子、铁离子和铝离子,镁离子、铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化镁、氢氧化铁不溶于氢氧化钠溶液中,但氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,偏铝酸根离子和二氧化碳能发生反应;
(3)加入的物质能和酸反应且不能引进杂质;
(4)I.从溶液中得到固体,需要加热浓缩、冷却结晶;
II.镁离子易水解生成氢氧化镁和氢离子,在氯化氢气流中加热该固体可以抑制其水解;
III.活泼金属采用电解的方法冶炼.
故答案为:光导纤维;
(2)滤液A中含有镁离子、铁离子和铝离子,镁离子、铁离子和铝离子都和氢氧化钠反应生成氢氧化物沉淀,氢氧化镁、氢氧化铁不溶于氢氧化钠溶液中,但氢氧化铝易溶于氢氧化钠溶液中生成偏铝酸根离子,偏铝酸根离子和二氧化碳反应生成氢氧化铝和碳酸氢根离子,离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)操作⑤中加入的物质能和盐酸反应,且不引进新的杂质,故选cd;
(4)Ⅰ.从溶液中得到固体,需要加热浓缩、冷却结晶,故答案为:加热浓缩、冷却结晶;
Ⅱ.镁离子易水解生成氢氧化镁和氢离子,在氯化氢气流中加热该固体时,氢离子浓度增大,抑制镁离子水解生成氢氧化镁,故答案为:Mg2++2H2O?Mg(OH)2+2H+,通入HCl,使C(H+)增大,抑制Mg2+的水解成Mg(OH)2,确保生成MgCl2;
Ⅲ. 镁是活泼金属,应采用电解其熔融盐的方法冶炼,所以工业上用电解熔融氯化镁的方法冶炼镁,反应方程式为:MgCl2
| ||
| 熔融 |
| ||
| 熔融 |

 名校课堂系列答案
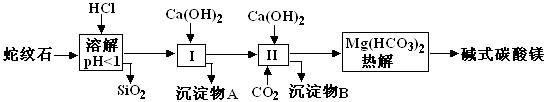
名校课堂系列答案蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如下:
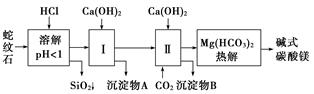
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是__________________。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)。
|
氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
开始沉淀pH |
1.5 |
3.3 |
9.4 |
Ca(OH)2不能过量,若Ca(OH)2过量可能会导致________溶解、________沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_____________________ ___________________________________________________(填入物质的化学式),
然后______________________________________________________________________(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是________(填写物质化学式)。
(5)现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量
②高温分解
③________________________________________________________________________
④________________________________________________________________________
⑤MgO称量
(6)18.2 g产品完全分解后,产生6.6 g CO2和8.0 g MgO,由此可知,产品的化学式中:
a=________,b=________,c=________。