题目内容
一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是( )
| A、c(M-)≥c(NH4+) |
| B、c(A-)≤c(M+) |
| C、若MA不水解,则c( OH-)<c(A-) |
| D、若MA水解,则c( OH-)>c(A-) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:如果一元酸HA为强电解质,则两溶液恰好反应时溶液显示中性,c(A-)=c(M+);若HA为为弱电解质,二者恰好反应生成强碱弱酸盐MA,溶液显示碱性,c(A-)<c(M+);无论MA水解还是不水解,由于A-离子水解程度较小,都一定存在c( OH-)<c(A-),据此进行解答.
解答:
解:若一元酸HA为强电解质,则两溶液恰好反应时溶液显示中性,c(A-)=c(M+);若HA为为弱电解质,二者恰好反应生成强碱弱酸盐MA,A-离子部分水解,溶液中c(A-)<c(M+),则溶液中离子浓度关系为:c(A-)≤c(M+),故A错误、B正确;
由于A-离子只是部分水解,其水解程度较小,无论MA水解还是不水解,溶液中离子浓度一定满足:c(A-)>c( OH-),故C正确、D错误,
故选BC.
由于A-离子只是部分水解,其水解程度较小,无论MA水解还是不水解,溶液中离子浓度一定满足:c(A-)>c( OH-),故C正确、D错误,
故选BC.
点评:本题考查了酸碱混合的定性判断、溶液中离子浓度定性比较,题目难度中等,注意掌握判断酸碱混合液的定性判断方法,明确盐的水解原理,能够根据电荷守恒、盐的水解原理等知识判断溶液中各离子浓度大小.

练习册系列答案
相关题目
下列物质中,导电性能最差的是( )
| A、石墨棒 | B、盐酸溶液 |
| C、熔融氢氧化钠 | D、固体氯化钾 |
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4,下列说法正确的是( )
| A、W、X、Y、Z的原子半径大小顺序是:W>X>Y>Z |
| B、Y的最高价氧化物对应水化物的酸性比Z的最高价氧化物对应水化物的酸性更强 |
| C、Y和Z形成的分子的空间构型可能是正四面体 |
| D、工业上用电解熔融的X和Z两元素组成的化合物来制取X的单质 |
下列结论中,正确的是( )
| A、摩尔是国际单位制的七个基本物理量之一 |
| B、0.012kg 12C约含有6.02×1023个碳原子 |
| C、1mol任何物质都含有6.02×1023个分子 |
| D、氢氧化钠的摩尔质量为40g |
下燃烧0.1mol两种气态烃的混合物,生成3.58L CO2(标准状况)和3.60g H2O,则混合气体中( )
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、一定无甲烷 |
| D、一定有丙烷 |
下列说法中正确的是( )
| A、中和热的测定实验中需要用的主要玻璃仪器有:二只大小相同的烧杯、二只大小相同的量筒、温度计、环形玻璃搅拌捧 |
| B、可以用保温杯代替烧杯做有关中和热测定的实验 |
| C、在测定中和热的实验中,至少需要测定并记录的温度是3次 |
| D、测定中和热实验中,若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高 |
2008年6月1日起,根据国务院要求所有超市、商场、集贸市场等商品零售场所实行塑料购物袋有偿使用.下列说法正确的是( )
| A、聚氯乙烯塑料属于烃类 |
| B、聚氯乙烯可以使酸性高锰酸钾溶液褪色 |
C、聚丙烯塑料的结构简式为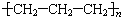 |
| D、聚丙烯是混合物 |
 某有机物的结构简式如图,下列说法正确的是( )
某有机物的结构简式如图,下列说法正确的是( )| A、该有机物1 mol 能与3 mol H2在镍作催化剂条件下发生加成反应 |
| B、该有机物1 mol 能与1 mol H2在镍作催化剂条件下发生加成反应 |
| C、该有机物能与NaHCO3反应放出CO2 |
| D、该有机物在一定条件下能发生银镜反应 |