题目内容
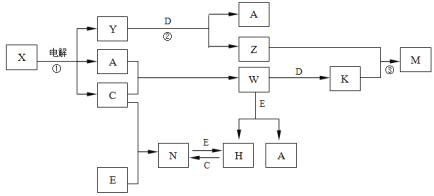
【题目】从海带中提取碘,有甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。请回答:
(1)步骤X使用分液漏斗前须检漏,检漏方法为_________。
(2)用右图所示装置进行蒸馏。指出右图所示实验装置中的任意两处错误:
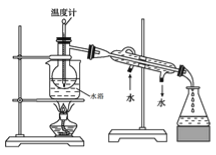
①___________;②__________。
(3)进行上述操作时,使用水浴加热更好的原因是___________;最后碘晶体在__________里聚集。
(4)下列有关步骤Y的说法,正确的是________。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
(5)方案乙在上层溶液中加入H2SO4溶液得到I2的水溶液发生的反应方程式是:_____________;
(6)操作Z的名称是____________。
(7)工业中采用方案乙从海带中提取碘,方案甲中采用蒸馏不合理,理由是______________。
【答案】(1)向分液漏斗中加入少量水,检查下口旋塞处是否漏水;将漏斗倒转过来,检查上口玻璃塞是否漏水
(2)①温度计水银球位置太低,应位于蒸馏烧瓶支管口处②烧杯加热未使用石棉网③冷凝管冷却水流方向反了
(3)均匀受热,易于控制温度;蒸馏烧瓶
(4)AB
(5)5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O(或NaI+NaIO+H2SO4=I2+Na2SO4+H2O)
(6)过滤或结晶过滤
(7)主要由于碘易升华,会导致碘的损失
【解析】
试题分析:(1)检查分液漏斗是否漏水的操作方法为:向分液漏斗中加入少量蒸馏水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是否漏水。
(2)蒸馏装置温度计水银球应在蒸馏烧瓶支管口处测定馏出成分的沸点,烧杯加热需要垫石棉网均匀加热,冷凝管水流方向应逆流,分析装置图可知,操作错误为:温度计插入液面以下,烧杯未垫石棉网,冷凝管水流方向顺流。
(3)碘易升华,需要水浴加热控制温度,水浴加热受热均匀,便于控制温度,碘单质生成蒸气,遇冷冷凝在蒸馏烧瓶中。故答案为:均匀受热,易于控制温度;蒸馏烧瓶;
(4)A.发生反应3I2+6NaOH═5NaI+NaIO3+3H2O中,需要浓氢氧化钠溶液,所以应控制NaOH溶液的浓度和体积,故A正确;B.根据反应3I2+6NaOH═5NaI+NaIO3+3H2O可知,步骤Y将碘转化成离子进入水层,故B正确;C.该操作的主要目的是将碘单质转化成碘酸钠、碘化钠,将碘转化成离子进入水层,不是除去有机杂质,故C错误;D.乙醇易溶于水和四氯化碳,将氢氧化钠换成乙醇,仍然无法分离出碘单质,故D错误。故答案为:AB;
(5)方案乙在上层溶液中是NaI和NaIO3,加入H2SO4溶液发生归中反应得到I2的水溶液,反应的化学方程式为:5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O。
(6)步骤Z将碘单质和水分离,由于碘单质不溶于水,可通过过滤操作完成。故答案为:过滤或结晶过滤;
(7)方案甲中采用蒸馏操作,由于碘单质容易升华,会导致碘单质损失,所以甲方案不合理。故答案为:碘单质易升华,会导致碘损失。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案【题目】下表各选项中,不能利用置换反应通过Y得到W的一组化合物是 ( )
选项化合物 | A | B | C | D |
Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
W | MgO | Al2O3 | CO | CuCl2 |
A. A B. B C. C D. D