题目内容
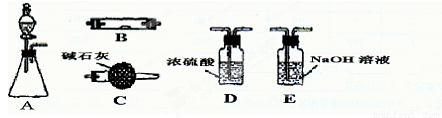
(15分)如图为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置(加热及固定装置均略去),仪器装置可任意选用,必要时可重复选择,请完成:
(1)若装置A的锥形瓶中装锌片,分液漏斗中装稀硫酸,则可验证H2的还原性并检验其氧化产物。
①若按顺序A→C→B→C连接仪器装置时,两次使用B装置,其中所盛的药品的化学式依次为CuO、 。
②检查装置的气密性后,加热装置B前必须进行的操作是_ 。
(2)若装置A的锥形瓶中装Na2O2,分液漏斗中装浓氨水,装置B中装红热的铂网可以进行氨的催化氧化;
①装置A的锥形瓶中反应的化学方程式为_ 、 ;
若气流按从左到右连接顺序A→D→B→B→C的方向,则B中氨的催化氧化反应方程式为 。
②装置B中除了观察到铂网保持红热外,还可能观察到的现象是 。
(3)若装置A的锥形瓶中装Na2SO3固体,分液漏斗中装70%的H2SO4溶液,装置B中装Na2O2固体,根据A→D→B→C的气流方向充分反应,探究SO2气体与Na2O2反应的是否生成O2。该实验中C装置的作用是 。
(1)①CuSO4 ②通一会儿氢气后,检验氢气的纯度
(2)①2Na2O2+2H2O=4NaOH+O2↑ NH3·H2O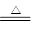 NH3↑+H2O 4NH3+5O2
NH3↑+H2O 4NH3+5O2 4NO+6H2O ②有红棕色气体出现
4NO+6H2O ②有红棕色气体出现
(3)防止空气中的水蒸气及CO2进入B装置与Na2O2反应生成氧气,同时吸收过量SO2气体,便于氧气的检验和防止污染空气
解析

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目