题目内容
(每空2分,共12分)
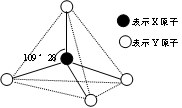
现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同)。A、B的晶体类型相同。单质A的同素异形体能与B物质发生置换反应。C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同。C、E、F的晶体类型相同,由E构成的物质常温下呈液态。请回答下列问题:
(1)写出单质A的同素异形体与B物质发生置换反应的化学方程式______ ;同主族的第四周期元素基态原子的外围电子排布式为 。
(2)上述六种物质或粒子的组成元素中有三种处于同一周期,请写出这三种元素第一电离能由大到小的顺序: 。
(3)上述六种物质或粒子中互为等电子体的是 (写出化学式)。
(4)F分子的中心原子杂化类型是 ,F易溶于E,其原因是
________________ 。
现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同)。A、B的晶体类型相同。单质A的同素异形体能与B物质发生置换反应。C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同。C、E、F的晶体类型相同,由E构成的物质常温下呈液态。请回答下列问题:

(1)写出单质A的同素异形体与B物质发生置换反应的化学方程式______ ;同主族的第四周期元素基态原子的外围电子排布式为 。
(2)上述六种物质或粒子的组成元素中有三种处于同一周期,请写出这三种元素第一电离能由大到小的顺序: 。
(3)上述六种物质或粒子中互为等电子体的是 (写出化学式)。
(4)F分子的中心原子杂化类型是 ,F易溶于E,其原因是
________________ 。
(1)SiO2 + 2C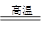 Si + 2CO ↑ 4S24P2 (2)N>O>C
Si + 2CO ↑ 4S24P2 (2)N>O>C
(3)CH4;NH4+ (4)SP3杂化,NH3和H2O为极性分子符合相似相溶原理,且NH3和H2O分子之间能形成氢键
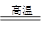 Si + 2CO ↑ 4S24P2 (2)N>O>C
Si + 2CO ↑ 4S24P2 (2)N>O>C(3)CH4;NH4+ (4)SP3杂化,NH3和H2O为极性分子符合相似相溶原理,且NH3和H2O分子之间能形成氢键
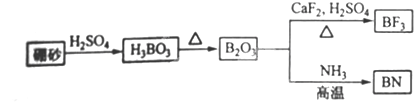
能形成键角为109°28′的单质是金刚石,即A是碳,在高温下碳能和二氧化硅发生反应生成单质硅和CO。常温下呈液态的是水,则E是水,所以D是NH4+,F是氨气,C是甲烷。
(1)反应式为SiO2 + 2C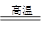 Si + 2CO ↑。第四周期第ⅣA元素是锗,其基态原子的外围电子排布式为4S24P2。
Si + 2CO ↑。第四周期第ⅣA元素是锗,其基态原子的外围电子排布式为4S24P2。
(2)处于同一周期的是C、N、O。非金属性越强第一电离能越大。但由于氮元素中2p轨道的单质是半充满状态,稳定性强,所以这三种元素第一电离能由大到小的顺序是N>O>C。
(3)电子数和原子数都相同的分子是等电子体,因此互为等电子体的是CH4和NH4+。
(4)氨气中中心原子的孤对电子是(5-1×3)÷2=1,所以是三角锥形结构,属于sp3杂化。由于NH3和H2O为极性分子符合相似相溶原理,且NH3和H2O分子之间能形成氢键,属于氨气极易溶于水。
(1)反应式为SiO2 + 2C
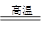 Si + 2CO ↑。第四周期第ⅣA元素是锗,其基态原子的外围电子排布式为4S24P2。
Si + 2CO ↑。第四周期第ⅣA元素是锗,其基态原子的外围电子排布式为4S24P2。(2)处于同一周期的是C、N、O。非金属性越强第一电离能越大。但由于氮元素中2p轨道的单质是半充满状态,稳定性强,所以这三种元素第一电离能由大到小的顺序是N>O>C。
(3)电子数和原子数都相同的分子是等电子体,因此互为等电子体的是CH4和NH4+。
(4)氨气中中心原子的孤对电子是(5-1×3)÷2=1,所以是三角锥形结构,属于sp3杂化。由于NH3和H2O为极性分子符合相似相溶原理,且NH3和H2O分子之间能形成氢键,属于氨气极易溶于水。

练习册系列答案
相关题目