题目内容
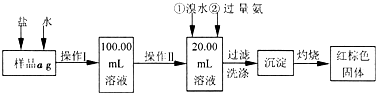
某氯化铁样品含有少量FeCl2杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行:
请根据上面流程,回答以下问题:
(1)操作 I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有
A.50mL烧杯 B.50mL量筒 C.25mL碱式滴定管 D.25mL酸式滴定管
(2)加入试剂①和②后发生反应的离子反应方程式为:
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是
(4)若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:
×100%
×100%.
(5)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是:

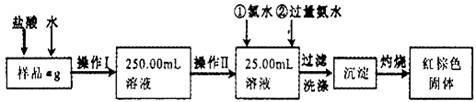
请根据上面流程,回答以下问题:
(1)操作 I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有
250mL容量瓶、胶头滴管
250mL容量瓶、胶头滴管
(填自选仪器名称),操作 II 必须用到的仪器是D
D
(从以下选项中选择,填编号).A.50mL烧杯 B.50mL量筒 C.25mL碱式滴定管 D.25mL酸式滴定管
(2)加入试剂①和②后发生反应的离子反应方程式为:
2Fe 2++Cl2=2Fe 3++2Cl-、Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
2Fe 2++Cl2=2Fe 3++2Cl-、Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是
再次加热,并置于干燥器中冷却,称量,直至连续两次质量差不超过0.1g为止
再次加热,并置于干燥器中冷却,称量,直至连续两次质量差不超过0.1g为止
.(4)若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:
| 7(W2-W1) |
| a |
| 7(W2-W1) |
| a |
(5)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的.他的理由是:
4Fe(OH)2+2H2O+O2=4Fe(OH)3
4Fe(OH)2+2H2O+O2=4Fe(OH)3
(用化学方程式表示)分析:本实验目的是测定铁的质量分数,采取的方法是使样品溶解、反应、最终生成氧化铁,然后通过氧化铁质量来求铁的质量分数.
(1)由图可知,操作I是将加入盐酸反应的溶液稀释成250.00mL溶液,故需要250mL的容量瓶;操作II是准确量取25.00mL的稀释后的溶液,故应需要滴定管;
(2)加氯水就是让+2价铁变为+3价,加氨水就是使+3价铁充分转化为Fe(OH)3沉淀;
(3)两次连续称量的质量相差不能超过0.1g才能说明分解完全,故应继续加热并称量;
(4)加热分解所得的物质是Fe2O3,其质量为(W2-W1)g,由于去25mL溶液,故250mL溶液可以得到Fe2O3质量为10(W2-W1)g,根据化学式计算铁元素的质量,再利用质量分数的定义计算原氧化铁样品中铁元素的质量分数;
(6)样品溶于水,不加氯水,生成的氢氧化亚铁在蒸干加热时氢氧化亚铁会迅速被氧气氧化为氢氧化铁,加热最终转化为Fe2O3,不影响铁元素质量分数的测定;
(1)由图可知,操作I是将加入盐酸反应的溶液稀释成250.00mL溶液,故需要250mL的容量瓶;操作II是准确量取25.00mL的稀释后的溶液,故应需要滴定管;
(2)加氯水就是让+2价铁变为+3价,加氨水就是使+3价铁充分转化为Fe(OH)3沉淀;
(3)两次连续称量的质量相差不能超过0.1g才能说明分解完全,故应继续加热并称量;
(4)加热分解所得的物质是Fe2O3,其质量为(W2-W1)g,由于去25mL溶液,故250mL溶液可以得到Fe2O3质量为10(W2-W1)g,根据化学式计算铁元素的质量,再利用质量分数的定义计算原氧化铁样品中铁元素的质量分数;
(6)样品溶于水,不加氯水,生成的氢氧化亚铁在蒸干加热时氢氧化亚铁会迅速被氧气氧化为氢氧化铁,加热最终转化为Fe2O3,不影响铁元素质量分数的测定;
解答:解:(1)由图可知,操作I是将加入盐酸反应的溶液稀释成250.00mL溶液,故需要250mL容量瓶、胶头滴管;操作II是准确量取25.00mL的稀释后的溶液,故应需要滴定管,
故答案为:250mL容量瓶、胶头滴管;D;
(2)加氯水就是让+2价铁变为+3价,发生反应为2Fe 2++Cl2=2Fe 3++2Cl-;加氨水就是使+3价铁充分转化为Fe(OH)3沉淀,发生反应为Fe3++3NH3H2O=Fe(OH)3↓+3NH4+;
故答案为:2Fe 2++Cl2=2Fe 3++2Cl-、Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
(3)两次连续称量的质量相差不能超过0.1g才能说明分解完全,故应继续加热并称量;
故答案为:继续加热,冷却至室温时,称量,直至两次连续称量质量差不超过0.1g;
(4)250mL溶液可以得到Fe2O3质量为10(W2-W1)g,铁元素的质量为10(W2-W1)g×
=7(W2-W1)g,所以原氧化铁样品中铁元素的质量分数=
×100%;
故答案为:
×100%;
(5)样品溶于水,不加氯水,生成的氢氧化亚铁在蒸干加热时氢氧化亚铁会迅速被氧气氧化为氢氧化铁,加热最终转化为Fe2O3,不影响铁元素质量分数的测定,故该方案可行,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
故答案为:250mL容量瓶、胶头滴管;D;
(2)加氯水就是让+2价铁变为+3价,发生反应为2Fe 2++Cl2=2Fe 3++2Cl-;加氨水就是使+3价铁充分转化为Fe(OH)3沉淀,发生反应为Fe3++3NH3H2O=Fe(OH)3↓+3NH4+;
故答案为:2Fe 2++Cl2=2Fe 3++2Cl-、Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+;
(3)两次连续称量的质量相差不能超过0.1g才能说明分解完全,故应继续加热并称量;
故答案为:继续加热,冷却至室温时,称量,直至两次连续称量质量差不超过0.1g;
(4)250mL溶液可以得到Fe2O3质量为10(W2-W1)g,铁元素的质量为10(W2-W1)g×
| 112 |
| 160 |
| 7(W2-W1) |
| a |
故答案为:
| 7(W2-W1) |
| a |
(5)样品溶于水,不加氯水,生成的氢氧化亚铁在蒸干加热时氢氧化亚铁会迅速被氧气氧化为氢氧化铁,加热最终转化为Fe2O3,不影响铁元素质量分数的测定,故该方案可行,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
点评:本题考查溶液配制、离子检验、对实验操作的理解与实验方案的评价、化学计算等,难度中等,清楚测定原理是解题的关键,是对所学知识的综合运用,需要学生具有扎实的基础与运用知识分析解决问题的能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行: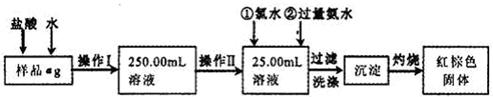
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯.玻璃棒.量筒外,还必须有____________ (填自选仪器名称),操作II必须用到的仪器是____________(填编号)。
| A.50mL烧杯 | B.50mL量筒 | C.25mL碱式滴定管 | D.25mL酸式滴定管 |
(3)检验沉淀是否已经洗涤干净的操作是________________________。
(4)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3g,则接下来还应进行的操作是____________。
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
(6)有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是________________________。(用化学方程式表示)