题目内容
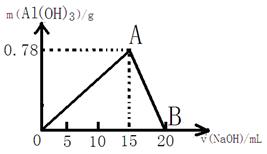
 向20mL某物质的量浓度的AlCl3溶液中滴加2mol/L NaOH溶液时,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH溶液的体积(mL)和所得沉淀的物质的量(mol)的关系如图所示.则:
向20mL某物质的量浓度的AlCl3溶液中滴加2mol/L NaOH溶液时,逐滴加入NaOH溶液直至过量.经测定,加入的NaOH溶液的体积(mL)和所得沉淀的物质的量(mol)的关系如图所示.则:(1)写出OA段发生反应的离子方程式:OA段
Al3++3OH-=Al(OH)3↓
Al3++3OH-=Al(OH)3↓
,图中线段OP:PB=3:1
3:1
.(2)计算原AlCl3溶液的物质的量浓度为
0.5
0.5
mol/L(3)图中A对应的横坐标为
15
15
mL(4)当加入5ml NaOH溶液时,产生沉淀量为
0.0033
0.0033
mol.(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,加入NaOH溶液的体积为
18.33
18.33
.分析:向20mL某物质的量浓度的AlCl3溶液中滴加2mol/L NaOH溶液时,逐滴加入NaOH溶液直至过量,过程中发生的反应为①Al3++3OH-=Al(OH)3↓,②Al(OH)3+OH-=AlO2-+2H2O,图象中OA段为发生反应①,AB段为氢氧化铝溶解发生反应②,依据各步反应分析判断,进行有关计算,
解答:解:(1)依据分析可知OA段发生的 反应是氯化铝和氢氧化钠反应生成氢氧化铝沉淀至最大量的过程,反应离子方程式为:Al3++3OH-=Al(OH)3↓; AB段发生的是氢氧化铝溶解在氢氧化钠溶液中至沉淀全部溶解,根据反应①Al3++3OH-=Al(OH)3↓,②Al(OH)3+OH-=AlO2-+2H2O得到生成最大量沉淀和沉淀全部溶解所消耗氢氧化钠物质的量为3:1,氢氧化钠溶液浓度一定,所以溶液体积比为3:1;故答案为:Al3++3OH-=Al(OH)3↓,3:1;
(2)图象中分析得到最大量氢氧化铝沉淀物质的量为0.01mol,所以氯化铝物质的量为0.01mol,溶液浓度=
=0.5mol/L;故答案为:0.5;
(3)图象中分析得到最大量氢氧化铝沉淀物质的量为0.01mol,所以消耗氢氧化钠物质的量为0.03mol,氢氧化钠溶液的体积=
=
=0.015L=15ml;故答案为:15;
(4)当加入5ml NaOH溶液时,产生沉淀量依据反应Al3++3OH-=Al(OH)3↓;计算得到:
Al3++3OH-=Al(OH)3↓;
1 3 1
0.005L×2mol/L n
n=0.0033mol;故答案为:0.0033;
(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,则发生反应Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,最大量沉淀为0.01mol,消耗氢氧化钠物质的量为0.03mol,溶解沉淀物质的量=0.01mol-0.0033mol=0.0067mol;消耗氢氧化钠0.0067mol;所以共消耗氢氧化钠物质的量=0.0067mol+0.03mol=0.0367mol;需要氢氧化钠溶液体积=
=0.01833L=18.33ml;故答案为:18.33;
(2)图象中分析得到最大量氢氧化铝沉淀物质的量为0.01mol,所以氯化铝物质的量为0.01mol,溶液浓度=
| 0.01mol |
| 0.02L |
(3)图象中分析得到最大量氢氧化铝沉淀物质的量为0.01mol,所以消耗氢氧化钠物质的量为0.03mol,氢氧化钠溶液的体积=
| n |
| c |
| 0.03mol |
| 2mol/L |
(4)当加入5ml NaOH溶液时,产生沉淀量依据反应Al3++3OH-=Al(OH)3↓;计算得到:
Al3++3OH-=Al(OH)3↓;
1 3 1
0.005L×2mol/L n
n=0.0033mol;故答案为:0.0033;
(5)当加入的NaOH溶液过量时,使最初生成的沉淀部分溶解,要得到与(4)中相同的沉淀量,则发生反应Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,最大量沉淀为0.01mol,消耗氢氧化钠物质的量为0.03mol,溶解沉淀物质的量=0.01mol-0.0033mol=0.0067mol;消耗氢氧化钠0.0067mol;所以共消耗氢氧化钠物质的量=0.0067mol+0.03mol=0.0367mol;需要氢氧化钠溶液体积=
| 0.0367mol |
| 2mol/L |
点评:本题考查了铝及其化合物性质的应用和计算,图象分析判断,理解氢氧化铝是两性氢氧化物能和强碱反应是解题关键,题目难度中等.

练习册系列答案
相关题目
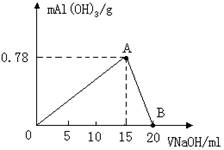
 向20mL某物质的量浓度的AlCl3溶液中滴入2mol/L NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
向20mL某物质的量浓度的AlCl3溶液中滴入2mol/L NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题: