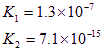题目内容
25 ℃时,几种弱酸的电离常数如下:
|
弱酸化学式 |
CH3COOH |
HCN |
H2S |
|
电离常数(25 ℃) |
1.8 ×10-5 |
4.9 ×10-10[来源:Zxxk.Com] |
K1=1.3 ×10-7 K2=7.1 ×10-15 |
下列说法正确的是( )
A. 等物质的量浓度的各溶液pH关系为: pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B. a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CN-),则a一定大于b
C. NaHS和Na2S混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
D. 某浓度HCN的水溶液pH=d,则其中c(OH-)=10-d mol/L
C
【解析】略

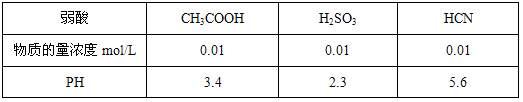
25°C时,几种弱酸溶液的PH如下表所示:
|
弱酸 |
CH3COOH |
H2SO3 |
HCN |
|
物质的量浓度mol/L |
0.01 |
0.01 |
0.01 |
|
PH |
3.4 |
2.3 |
5.6 |
下列有关说法正确的是
A.相同PH的CH3COOH与HCN溶液中水电离的氢离子浓度CH3COOH溶液中的大
B.物质的量浓度相同的CH3COONa与NaCN溶液中,各离子浓度之和两者相等。
C.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在
如下关系:Ka ·K = Kw
D.0.01mol/L的Na2SO3溶液与0.01mol/L的CH3COONa溶液相比,一定是后者的碱性强
25°C时,几种弱酸溶液的PH如下表所示:
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| PH | 3.4 | 2.3 | 5.6 |
下列有关说法正确的是
- A.相同PH的CH3COOH与HCN溶液中水电离的氢离子浓度CH3COOH溶液中的大
- B.物质的量浓度相同的CH3COONa与NaCN溶液中,各离子浓度之和两者相等
- C.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在如下关系:Ka ·K = Kw
- D.0.01mol/L的Na2SO3溶液与0.01mol/L的CH3COONa溶液相比,一定是后者的碱性强
25°C时,几种弱酸的电离常数如下
| 弱酸化学式 | CH3COOH | HCN | H2S |
| 电离常数(25°C) | 1.8 |
|
|
25°时,下列说法正确的是 ( )
A.等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定大于b
C.某浓度HCN的水溶液pH=d,则其中c(OH-)=10-dmol/L
D.NaHS和Na2S混合溶液中,一定存在c(Na+)+c(H+)===c(OH-)+c(HS-)+2c
(S2-)
25°C时,几种弱酸溶液的PH如下表所示:
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| PH | 3.4 | 2.3 | 5.6 |
A.相同PH的CH3COOH与HCN溶液中水电离的氢离子浓度CH3COOH溶液中的大
B.物质的量浓度相同的CH3COONa与NaCN溶液中,各离子浓度之和两者相等。
C.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在
如下关系:Ka ·K = Kw
D.0.01mol/L的Na2SO3溶液与0.01mol/L的CH3COONa溶液相比,一定是后者的碱性强