题目内容
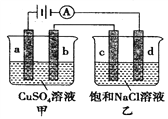
【题目】如图所示,是原电池的装置图。请回答:

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为____;
(2)若C为CuCl2溶液,Zn是负极,Cu极发生____反应,电极反应为____。
(3)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如图:
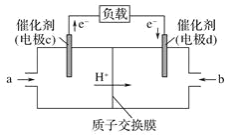
电池总反应为2CH3OH+3O2=2CO2+4H2O,c电极为____极,电极反应方程式为____。若线路中转移2mol电子,则消耗的O2在标准状况下的体积为____ L。
【答案】2H++2e-=H2↑ 还原 Cu2++2e-=Cu 负 CH3OH6e-+H2O=CO2↑+6H+ 11.2
【解析】
(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,电极反应为Fe-2e-=Fe2+,A为正极,溶液中氢离子得到电子生成氢气,电极反应为2H++2e-=H2↑;
(2)锌、铜和CuCl2溶液构成的原电池中,锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,导致锌逐渐溶解,电极反应式为Zn-2e-=Zn2+,铜作正极,正极上铜离子得电子发生还原反应而析出铜单质,电极反应式为Cu2++2e-=Cu;
(3)根据图中电子流向可知c为负极,是甲醇发生氧化反应,电极反应式为CH3OH-6e-+H2O=CO2↑+6H+;1mol氧气在反应中得到4mol电子,因此若线路中转移2mol电子时消耗氧气0.5mol,在标准状况下的体积为0.5mol×22.4L/mol=11.2L。

练习册系列答案
相关题目