题目内容
国务院强调,调水必须坚持“三先三后”的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的Mg2+、Al3+、Cu2+、Ag+。试分析回答下列问题。
(1)该废液中可能大量存在的一种阴离子是________(填字母代号)。
A.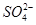 B.
B.
C.Cl- D.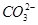
(2)检测废液中铝元素的含量,需将其从废液样品中分离出来,所用的试剂可以是________溶液,铝元素发生变化的离子方程式是____________________________________________。
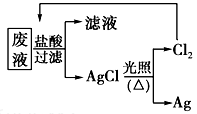
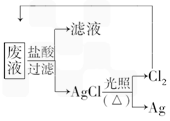
(3)为了回收废液中的金属银,某同学设计了如下方案:
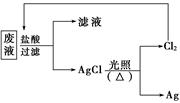
若依该方案获得Ag 108 g,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的H2的体积为____________。(Ag的相对原子质量为108)
(1)B (2)NaOH或KOH Al3++4OH-=== +2H2O[或Al3++3OH-===Al(OH)3↓,
+2H2O[或Al3++3OH-===Al(OH)3↓,
Al(OH)3+OH-=== +2H2O] (3)11.2 L
+2H2O] (3)11.2 L
【解析】
试题分析:(1)从选项可以看出,能与Ag+大量共存的阴离子只有 ,故选B。
,故选B。
(2)要想从溶液中分离出Al3+,一般需要沉淀其他离子而其本身不沉淀,要想达到这个目的,只能用强碱NaOH或KOH,离子方程式见答案。
(3)由质量守恒和关系式可得:Ag~AgCl~HCl~ Cl2~
Cl2~ H2,故n(H2)=
H2,故n(H2)= n(Ag)。
n(Ag)。
n(H2)= =
= mol
mol
V(H2)= mol×22.4
L·mol-1=11.2 L。
mol×22.4
L·mol-1=11.2 L。
考点:考查物质的分离、提纯、离子共存的正误判断以及化学计算
点评:该题是中等难度的试题,也是高考中的常见题型,试题基础性强,侧重考查学生分析问题、解决问题的能力。该题有利于培养学生的规范答题能力以及逻辑思维能力。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
| |||||||||||||||||||||||||
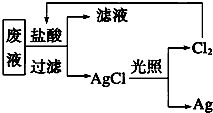 国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题:
国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污、生态环境保护与调水作为一个完整的系统来分析的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.试分析回答下列问题: