题目内容
(1)在实验室里可以用浓盐酸跟二氧化锰起反应制取氯气,反应的化学方程式为:______________________________________________________。
(2)往过氧化氢溶液中加入二氧化锰粉末可以产生氧气,此反应中二氧化锰的作用是_____________。
(3)在SO2、CaO、D2、HCl、Na2CO3五种纯物质中,属于共价化合物的是_________________________;含非极性键的是_______________。
(4)已知:2SO2 + O2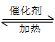 2SO3 。向一密闭容器中充入SO2 与18O2 ,反应一段时间后,含18O的物质是_______________________。
2SO3 。向一密闭容器中充入SO2 与18O2 ,反应一段时间后,含18O的物质是_______________________。
(5)如下反应:
① Zn + CuSO4 = ZnSO4 +Cu
② NaOH + HCl = NaCl + H2O
③ 4Al + 3O2 = 2Al2O3
④ Na2CO3 + H2SO4 = Na2SO4 + CO2↑+ H2O
其中可以设计成原电池的是_______________(写序号)。
(2)往过氧化氢溶液中加入二氧化锰粉末可以产生氧气,此反应中二氧化锰的作用是_____________。
(3)在SO2、CaO、D2、HCl、Na2CO3五种纯物质中,属于共价化合物的是_________________________;含非极性键的是_______________。
(4)已知:2SO2 + O2
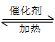 2SO3 。向一密闭容器中充入SO2 与18O2 ,反应一段时间后,含18O的物质是_______________________。
2SO3 。向一密闭容器中充入SO2 与18O2 ,反应一段时间后,含18O的物质是_______________________。(5)如下反应:
① Zn + CuSO4 = ZnSO4 +Cu
② NaOH + HCl = NaCl + H2O
③ 4Al + 3O2 = 2Al2O3
④ Na2CO3 + H2SO4 = Na2SO4 + CO2↑+ H2O
其中可以设计成原电池的是_______________(写序号)。
(1)MnO2 + 4HCl(浓)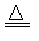 MnCl2 + Cl2↑+2H2O
MnCl2 + Cl2↑+2H2O
(2)作催化剂
(3)SO2、HCl;D2
(4)O2、SO2、SO3
(5)①③
 MnCl2 + Cl2↑+2H2O
MnCl2 + Cl2↑+2H2O(2)作催化剂
(3)SO2、HCl;D2
(4)O2、SO2、SO3
(5)①③

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
(10分)在实验室里可以用如下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质(固定装置略去)。图中①为制取氯气的装置;②试管中装有15mL30%KOH溶液,并置于热水中,制取氯酸钾;③试管中装有15 mL 8%NaOH溶液,并置于冰水中;④中装有紫色石蕊试液。

(1)③试管中制取次氯酸钠的化学方程式为
(2)实验中可观察到④试管中溶液的颜色发生如下变化,填写表格。
|
实验现象 |
原因 |
|
溶液最初从紫色变为 色 |
氯气与水反应生成的HCl使石蕊试液变红 |
|
随后溶液逐渐变为无色 |
|
|
最后溶液从无色逐渐变为 色 |
|
(3)此实验有一个明显的不足之处,应如何改进?
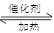 2 SO3。向一密闭容器中充入SO2与18O2,反应一段时间后,含18O的物质是_______________________。
2 SO3。向一密闭容器中充入SO2与18O2,反应一段时间后,含18O的物质是_______________________。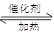 2 SO3 。向一密闭容器中充入SO2 与18O2
,反应一段时间后,含18O的物质是_______________________。
2 SO3 。向一密闭容器中充入SO2 与18O2
,反应一段时间后,含18O的物质是_______________________。