题目内容
【题目】(1)下列装置属于原电池的是___________;
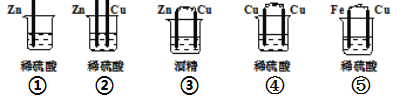
(2)在选出的原电池中,______ 是负极,发生______(氧化、还原) 反应 ,______ 是正极 ,该极的现象___________________________;
(3)在该原电池的内电路中,硫酸根离子移向_________(正、负)极。
(4)此原电池反应的化学方程式为___________________________。
【答案】⑤ Fe 氧化 Cu 有气泡产生 负 Fe+H2SO4= FeSO4+ H2↑
【解析】
(1)①中没有两个活泼性不同的电极,所以不能构成原电池,故①错误;
②没有构成闭合回路,所以不能构成原电池,故②错误;
③酒精为非电解质溶液,所以不能构成原电池,故错③误;
④电极材料相同,所以不能构成原电池,故④错误;
⑤符合原电池的构成条件,所以能构成原电池,故⑤正确。
故答案为:⑤。
(2)该装置中,铁易失电子而作负极,铜作正极,负极上铁失电子生成亚铁离子发生氧化反应,正极上氢离子得电子发生还原反应而生成氢气,所以有气泡生成,故答案为:氧化,Cu,有气泡产生。
(3)原电池内电路中,硫酸根是阴离子,阴离子移向负极,故答案为:负。
(4)该原电池中,铁失电子生成亚铁离子,正极上氢离子得电子生成氢气,所以电池反应式为:Fe+H2SO4=FeSO4+H2↑,故答案为:Fe+H2SO4=FeSO4+H2↑。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目