题目内容
【题目】有下列物质:①O2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦MgCl2 ⑧H2O2 ⑨NH4Cl ⑩N2,回答下列问题:
(1)只含有极性键的是__;只含有非极性键的是__;只含有离子键的离子化合物是___;含有非极性键的离子化合物是____。(均填序号)
(2)写出⑤、⑨的电子式_____、______
(3)用电子式表示MgCl2的形成过程:____________。
【答案】②③ ①⑩ ④⑦ ⑤ ![]()

![]()
【解析】
(1)①O2中只含非极性键,属于单质;
②CO2中只含极性键,属于共价化合物;
③NH3中只含极性键,属于共价化合物;
④Na2O中只含离子键,属于离子化合物;
⑤Na2O2中含有离子键和非极性键,属于离子键化合物;
⑥NaOH中含有离子键和极性键,属于离子键化合物;
⑦MgCl2中只含离子键,属于离子化合物;
⑧H2O2含有H-O极性键和O-O非极性键,属于共价化合物;
⑨NH4Cl中含有离子键和极性键,属于离子键化合物;
⑩N2中只含非极性键,属于单质。
(1)只含有极性键的是②③;只含有非极性键的是①⑩;只含有离子键的离子化合物是④⑦;含有非极性键的离子化合物是⑤,故答案为:②③;①⑩;④⑦;⑤。
(2)⑤Na2O2为含有共价键的离子化合物,钠原子与过氧根离子之间形成离子键,过氧根离子中氧原子与氧原子之间形成共价键,电子式为![]() ,⑨NH4Cl为含有共价键的离子化合物,铵根离子与氯离子之间形成离子键,铵根离子中N原子与H原子之间形成共价键,电子式为
,⑨NH4Cl为含有共价键的离子化合物,铵根离子与氯离子之间形成离子键,铵根离子中N原子与H原子之间形成共价键,电子式为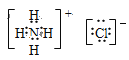 ,故答案为:
,故答案为:![]() ,
,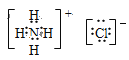 。
。
(3)MgCl2为离子化合物,用电子式表示其形成过程为:![]() ,故答案为:
,故答案为:![]() 。
。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
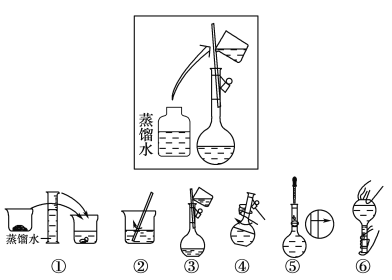
课堂练加测系列答案【题目】一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料制取醋酸镍的工艺流程图如下:
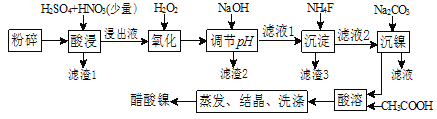
相关离子生成氢氧化物的pH和相关物质的溶解性如下表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时溶解性(H2O) |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 |
A13+ | 3.0 | 5.0 | CaF2 | 难溶 |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.60×10-6 |
(1)调节pH步骤中,溶液pH的调节范围是______________。
(2)滤渣1和滤渣3主要成分的化学式分别是_____________、__________________。
(3)酸浸过程中,1 molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式________________________________。
(4)沉镍过程中,若c(Ni2+)=2.0mol·L-1,欲使100mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5 mol·L-1,则需要加入Na2CO3固体的质量最少为_________g。(保留小数点后1位有效数字)。
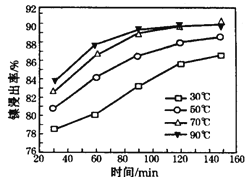
(5)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间为_______________。