��Ŀ����
����Ŀ�������������ʹ�õĽ���֮һ��������ѧ֪ʶ���ش��������⡣
��1������Fe(OH)3�����FeCl3��Һ�ķ����� ��
��2�����ӹ�ҵ��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ������ӡˢ��·�壬��д��FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ�� ��
��3��ij�о���ѧϰС��Ϊ�ⶨFeCl3��ʴͭ��������Һ����ɣ�����������ʵ�飺��ȡ����������Һ������KSCN��Һ����ɫ�������Һ�к��еĽ����������� ������Һ��ɵIJⶨ��ȡ50.0mL������Һ������������AgNO3��Һ����21.525g��ɫ����������Һ��c(Cl��)�� mol��L��1��
����֤����Һ�к���Fe2+����ȷ��ʵ�鷽���� ��
A���۲���Һ�Ƿ��dz��ɫ
B��ȡ������Һ���������Ը��������Һ������ɫ��֤������Fe2+
C��ȡ������Һ��������ˮ���ٵ���KSCN��Һ������Ѫ��ɫ��֤��ԭ��Һ�к���Fe2+
��4������ʦ��������ӡˢ��·��ķ�ˮ�л���ͭ�������FeCl3��Һ��������·�����
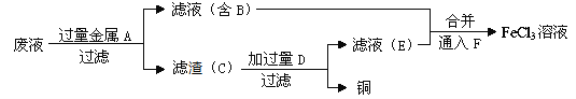
������C�Ļ�ѧʽΪ ��
�ڼӹ���D������Ӧ�����ӷ���Ϊ ��
��ͨ��F������Ӧ�Ļ�ѧ����ʽΪ_________________________��
���𰸡���1����ƽ�й��������ַ�ɢϵ���������
��2��2Fe3++Cu=2Fe2++Cu2+��2�֣�
��3����Fe3+ ��Fe2+��Cu2+ ��3 ��B��2�֣�
��4����Fe��Cu��Fe+2H+=Fe2++H2����2FeCl2+Cl2=2FeCl3��2�֣�
��������
���������
��1����FeCl3��Һ����Һ�����������Fe(OH)3�����ǽ��壬�ж�����������Լ���FeCl3��Һ��Fe(OH)3�����������Ч���ǹ۲��Ƿ�����˶��������ЧӦ�����ʴ�Ϊ����ƽ�й��������ַ�ɢϵ���������
��2��ͭ���Ȼ�����Ӧ�����Ȼ�ͭ���Ȼ���������Ӧ�����ӷ���ʽΪ��Cu+2Fe3+=Cu2++2Fe2+��
��3����FeCl3��Һ��ͭ��Ӧ�����ӷ���ʽ�ǣ�2Fe3++Cu�T2Fe2++Cu2+�����ڵ���KSCN��Һ�ʺ�ɫ��֤����Һ��Fe3+��ʣ�࣬��Һ�к��еĽ����������ǣ�Fe3+��Fe2+��Cu2+���ʴ�Ϊ��Fe3+��Fe2+��Cu2+�� �ڳ���21.525g���Ȼ��������ʵ�����0.15mol����Һ��c(Cl-)=![]() =3.0mol/L���ʴ�Ϊ��3.0����A���۲���Һ�Ƿ��dz��ɫ������֤������A����B�����Թ��м�����Һ���������Ը��������Һ������ɫ��֤������Fe2+����B��ȷ��C���Թ��м�����Һ��������ˮ���ٵ���KSCN��Һ������Ѫ��ɫ��֤��ԭ��Һ�к���Fe2+��Ӧ�����ȼ������軯�أ�����ɫ���ټ�����ˮ������ʾ��ɫ��֤�����������ӣ���C����ѡB��
=3.0mol/L���ʴ�Ϊ��3.0����A���۲���Һ�Ƿ��dz��ɫ������֤������A����B�����Թ��м�����Һ���������Ը��������Һ������ɫ��֤������Fe2+����B��ȷ��C���Թ��м�����Һ��������ˮ���ٵ���KSCN��Һ������Ѫ��ɫ��֤��ԭ��Һ�к���Fe2+��Ӧ�����ȼ������軯�أ�����ɫ���ټ�����ˮ������ʾ��ɫ��֤�����������ӣ���C����ѡB��
��4����ȡ�����Ȼ�����Һ������A��������ҺB���Ȼ�������Һ�������������������C������ͭ����ȡ�����Ȼ������ܽ�����D����Ӧ��������ɴ˿�֪������C�Ļ�ѧʽΪFe��Cu���ʴ�Ϊ��Fe��Cu���ڼӹ������ᷢ����Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2�����ʴ�Ϊ��Fe+2H+=Fe2++H2�������ǽ������������������������ӣ���Ӧ����ʽ�ǣ�2FeCl2+Cl2=2FeCl3���ʴ�Ϊ��2FeCl2+Cl2=2FeCl3��

 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�