题目内容
15.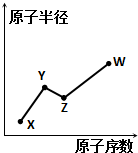 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | Y、W的最简单氢化物的水溶液能相互反应 | |
| C. | X、W可形成离子化合物XW | |
| D. | X、Z、W形成的化合物均为强酸 |
分析 X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,结合元素化合物性质解答.
解答 解:X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,
A.Y为N,Z为O,二者处于第二周期,W为Cl,处于第三周期,故A错误;
B.氨气与HCl反应生成氯化铵,故B正确;
C.X、W可形成共价化合物HCl,故C错误;
D.X、Z、W形成的化合物中HClO为弱酸,故D错误,
故选B.
点评 本题考查位置结构性质关系等,难度中等,推断元素是解题的关键,注意对元素周期律的理解与运用.

练习册系列答案
相关题目
16.废电池必须进行集中处理的首要原因是( )
| A. | 防止电池中汞、镉和铅等重金属离子污染土壤和水源 | |
| B. | 回收利用石墨电极和金属材料 | |
| C. | 充电后可再使用 | |
| D. | 防止电池中的电解质溶液腐蚀其他物品 |
10.在100mL混合液中,HNO3和H2SO4物质的量浓度分别是0.4mol/L和0.1mol/L,向该混合液中加入1.92gCu粉,加热充分反应后,所得气体在标况下的体积约为( )
| A. | 0.336L | B. | 0.448L | C. | 0.896 L | D. | 1.344L |
20.下列各物质中,最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 丙烯和环己烷 | B. | 乙烯和己烯 | C. | 乙烷和苯 | D. | 正丁烷和异丁烷 |
4.迷迭香酸是从蜂花属植物中提取得到的酸性物质如图.下列取叙述正确的是( )
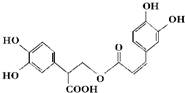

| A. | 迷迭香酸属于芳香烃 | |
| B. | 1 mol迷迭香酸最多能和9 mol氢气发生加成反应 | |
| C. | 迷迭香酸可以发生水解反应、取代反应和酯化反应 | |
| D. | 1 mol迷迭香酸最多能和含5 mol NaOH的水溶液完全反应 |
5.下列有关化学反应表达正确的是( )
| A. | 甲醛溶液与足量的银氨溶液共热:HClO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O | |
| B. | 同位素示踪法研究酯化反应:CH3COOH+H18OCH2CH3$?_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH3+H218O | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
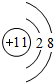 ,BD4的电子式为
,BD4的电子式为 .
.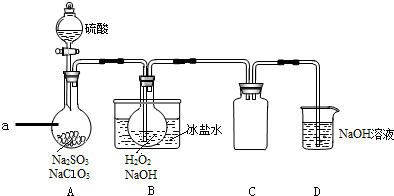
 “有钱就是这么任性”是2014年流行起来的网络用语.用来调侃有钱人令网友大跌眼镜的做事风格.甲、乙两种有机物分子的键线式如图,很像“任性”的汉语拼音缩写.
“有钱就是这么任性”是2014年流行起来的网络用语.用来调侃有钱人令网友大跌眼镜的做事风格.甲、乙两种有机物分子的键线式如图,很像“任性”的汉语拼音缩写.