题目内容
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大 |
| B.39g Z2Y2中含有的离子数约为1.204×1024 |
| C.元素Z、R的氧化物的水化物之间相互反应生成的盐一定是正盐 |
| D.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
D
解析试题分析:由题意知X为H元素,Y为O元素,R与Y处于同一族,R为S元素,Z、W、R处于同一周期,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,所以Z、W分别为Na、Al。A、元素Y、Z、W形成的离子具有相同电子层结构,其离子半径应依次减小,错误;B、39g Na2O2的物质的量是0.5mol,阴离子为0.5mol,阳离子为1mol,所以含有的离子数约为1.5×6.02×1023=9.03×1023,错误;C、S与Na的氧化物的水化物之间相互反应生成的盐可能是正盐,也可能是酸式盐,错误;D、O的非金属性强于S的非金属性,所以H2O的热稳定性大于H2S的热稳定性,正确,答案选D。
考点:考查元素原子结构与元素周期律的关系

 阅读快车系列答案
阅读快车系列答案下列有关物质性质的比较,正确的是
| A.热稳定性:HF<HCl<HBr | B.微粒半径: O2->Mg2+>Cl- |
| C.第一电离能:Si>Al>Mg | D.电负性:Si>Al>Mg |
X、Y、Z为短周期元素,这些元素原子的最外层电子数分别为1、4、6,则由这三种元素组成的化合物的化学式可能是
| A.XYZ | B.X3YZ | C.XYZ2 | D.X2YZ3 |
AZX与A+1ZX+的两种微粒,下列叙述正确的是
| A.一定都是由质子、中子、电子组成的 |
| B.化学性质几乎完全相同 |
| C.核电荷数和核外电子数一定相等 |
| D.质子数一定相同,质量数和中子数一定不相同 |
X、Y、Z是三种短周期金属元素,原子序数依次增大,单质的物质的量分别为n(X)、n(Y)、n(Z),它们与足量盐酸反应产生的氢气体积(标准状况下)为V(H2)X、V(H2)Y、V(H2)Z,且n(X)=n(Y)=n(Z),2V(H2)X=V(H2)Y+V(H2)Z。下列说法正确的是( )
| A.X、Y、Z一定处于同一周期 |
| B.X可能是镁 |
| C.Y和Z的最高价氧化物对应的水化物在一定条件下能反应 |
| D.工业上冶炼X、Y、Z通常是用热还原法制得 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是( )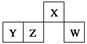
| A.原子半径:rW>rZ>rY>rX |
| B.含Y元素的盐溶液显酸性 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.X与氢元素组成的化合物XH5与水反应可产生两种气体 |
X、Y、Z、W、R属于短周期元素。已知它们都不是稀有气体元素,X的原子半径最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2∶1。下列叙述错误的是( )
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1∶2 |
| B.Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 |
| C.Z、W、R最高价氧化物对应水化物的酸性强弱顺序:R>W>Z |
| D.Y分别与Z、W、R以两种元素组成的常见化合物有5种 |
钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是( )
| A.K是银白色金属,硬度大,熔点高 |
| B.K在空气可以被空气中的氧气所氧化,且产物只有K2O |
| C.K与水能够反应,但不如Na与水的反应剧烈,产物都有氢气 |
| D.K也可以与氯气反应,且比Na与氯气的反应剧烈 |
某元素的原子核外有3个电子层,最外层有4个电子,该原子核内的质子数为( )。
| A.14 | B.15 | C.16 | D.17 |