题目内容
在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题:
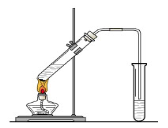
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是: 。
(2)饱和碳酸钠溶液的主要作用 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,其目的是 。
(4)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
⑥混合物水中的18O的物质的量不再变化

(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是: 。
(2)饱和碳酸钠溶液的主要作用 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,其目的是 。
(4)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
⑥混合物水中的18O的物质的量不再变化
(8分)(1)先加入乙醇后缓慢注入硫酸,不断搅拌,冷却后加醋酸
(2) 除去混在酯中的乙酸,溶解乙醇,利于酯的分层析出 。
(3) 防止倒吸 (4)②④⑤⑥
(2) 除去混在酯中的乙酸,溶解乙醇,利于酯的分层析出 。
(3) 防止倒吸 (4)②④⑤⑥
试题分析:(1)由于浓硫酸溶于水会放出大量的热量,且密度大于水的,所以在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是先加入乙醇后缓慢注入硫酸,不断搅拌,冷却后加醋酸。
(2))由于生成的乙酸乙酯中混有乙酸和乙醇,所以饱和碳酸钠溶液的作用是反应乙酸、溶解乙醇、降低乙酸乙酯溶解度,利于酯的分层析出,且便于闻到乙酸乙酯的香味。
(3)由于乙酸和乙醇都是和水互溶的,所以导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中的目是防止倒吸。
(4)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以④⑤⑥正确;①③中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此①③中的关系始终是成立,不正确;②中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确,答案选②④⑤⑥。
点评:该题是高考中的常见考点,属于中等难度的试题。试题难易适中,侧重对学生基础性知识的巩固与训练,有助于培养学生综合实验能力。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。该题的难点是平衡状态的判断。

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
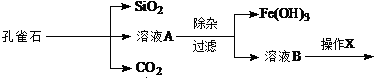
 为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下:
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如下: