题目内容
设计一个只用氯化钡溶液及试管鉴别亚硫酸钠溶液和稀硫酸的实验,简要写出实验过程和实验结论(亚硫酸钡是白色固体)。
各取一定量的两种未知溶液分别放入两支试管里,然后滴加BaCl2溶液,两试管内都出现沉淀。然后将一支试管内的溶液倒入另一支试管内,若沉淀溶解,则沉淀物为亚硫酸钡,溶液为盐酸。生成此沉淀的原未知溶液为亚硫酸钠,另一溶液为稀硫酸。若沉淀不溶解,则生成此沉淀的原溶液为稀硫酸,另一溶液为亚硫酸钠。
解析:设计实验的思路可以从两个反应产生:
BaCl2+H2SO4====BaSO4↓+2HCl
BaCl2+Na2SO3====BaSO3↓+2NaCl
从两个反应的比较中可以看出,前一个反应中生成的溶液,能将后一个反应中生成的沉淀溶解,所以实验方法就是将一支试管内的溶液倒入另一支试管内,通过观察沉淀是否溶解来判断沉淀物和溶液的组成,从而确定原未知溶液的成分。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
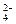 、SO
、SO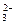 、S2-、Cl-、Br-、I-、NO
、S2-、Cl-、Br-、I-、NO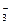 、Na+、Mg2+等离子.
、Na+、Mg2+等离子.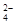 、SO
、SO 、S2-、Cl-、Br-、I-、NO、Na+、Mg2+等离子.
、S2-、Cl-、Br-、I-、NO、Na+、Mg2+等离子.