题目内容
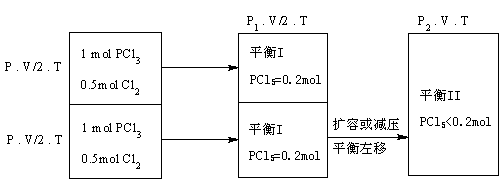
一定温度下,将2mol PCl3和 1mol Cl2充入容积不变的密闭容器中,在一定条件下反应:PCl3(g)+Cl2(g) PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )
PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )
 PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )
PCl5(g)。达平衡后,PCl5为0.4mol。若此时再移走1mol PCl3和0.5mol Cl2,相同温度下重新达到平衡,PCl5的物质的量为( )| A.0.4mol |
| B.0.2mol |
| C.0.2mol<x<0.4mol |
| D.<0.2mol |
D
对原平衡移走1mol PCl3和0.5mol Cl2,相当于起始投料量减为原投料量的一半,若PCl3的转化率不变,即假设最终的平衡状态与原平衡相同,PCl5的物质的量应为0.2mol。但移走反应物相当于减小浓度(减压)或增大容积,平衡会向增大压强的方向进行,所以平衡左移,PCl5消耗更多,其平衡物质的量<0.2mol。


练习册系列答案
相关题目
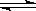 4C+6D。达到平衡时,测得A的转化率大于B的转化率。则n的取值范围正确的是
4C+6D。达到平衡时,测得A的转化率大于B的转化率。则n的取值范围正确的是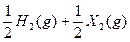

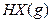 的平衡常数为9。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于
的平衡常数为9。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于 C(g)+D(g)
C(g)+D(g)
 2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。
2C + D + Q,此时,A,B,C的物质的量均为amol,而D的物质的量为dmol。改变a的取值,再通过改变反应的条件,可以使反应重新达到平衡,并限定达到新的平衡时,D的物质的量只允许在d/2与2d之间变化,则a的取值范围应是__________________________(用a和d的关系式表示)。 2NO2并达到平衡,此时测得容器内混合气体的密度比原来减少1/3(温度和压强不变)。计算:
2NO2并达到平衡,此时测得容器内混合气体的密度比原来减少1/3(温度和压强不变)。计算: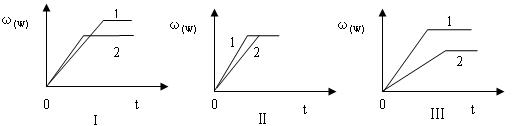
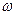 (W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是( )
(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是( )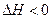
 2NH3。当反应达平衡时,恢复到原温度和压强下,测得NH3的体积分数为40%,则N2在平衡混合体系中的体积分数为( )
2NH3。当反应达平衡时,恢复到原温度和压强下,测得NH3的体积分数为40%,则N2在平衡混合体系中的体积分数为( )