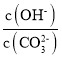题目内容
【题目】某温度下,向一定体积![]() 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中
醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中![]()
![]() 与pH的变化关系如图所示,则
与pH的变化关系如图所示,则
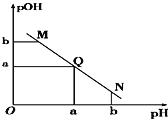
A.M点所示溶液导电能力强于Q点
B.N点所示溶液中![]()
C.M点和N点所示溶液中水的电离程度不相同
D.Q点消耗NaOH溶液的体积小于醋酸溶液的体积
【答案】D
【解析】
根据题给信息及图可知,向一定体积![]() 醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pH逐渐增大。Q点时,
醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液pH逐渐增大。Q点时,![]() ,溶液呈中性,M点时,溶液呈酸性,
,溶液呈中性,M点时,溶液呈酸性,![]() 有剩余,N点时,溶液呈碱性。
有剩余,N点时,溶液呈碱性。
![]() 点的
点的![]() ,溶液为中性,由于醋酸是弱酸,电离程度很小,离子浓度也较小,醋酸溶液中离子浓度小于Q点溶液中离子浓度,故M点溶液的导电能力较弱,故A错误;
,溶液为中性,由于醋酸是弱酸,电离程度很小,离子浓度也较小,醋酸溶液中离子浓度小于Q点溶液中离子浓度,故M点溶液的导电能力较弱,故A错误;
B. N点所示溶液为碱性,则![]() ,由电荷守恒:
,由电荷守恒:![]() ,可得:
,可得:![]() ,故B错误;
,故B错误;
C. M点的溶液中氢氧根离子源于水的电离,N点氢氧根离子也源于水的电离,由于M点的![]() 浓度等于N点的
浓度等于N点的![]() 浓度,所以两点水电离程度相同,故C错误;
浓度,所以两点水电离程度相同,故C错误;
D. Q点的![]() ,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性,所以Q点醋酸过量,所加NaOH溶液体积小于醋酸溶液的体积,故D正确;
,溶液为中性,而两者等体积混合后生成醋酸钠,水解显碱性,所以Q点醋酸过量,所加NaOH溶液体积小于醋酸溶液的体积,故D正确;
答案选D。

练习册系列答案
相关题目