题目内容
【题目】如下图所示,向A、B中均充入1mol X、l mol Y,起始时A、B的体积都等于1L。在同温、同压和催化剂存在的条件下,关闭活塞K,使两容器中都发生下述反应:X(g)+Y(g) ![]() 2Z(g)+W(g) ΔH <0,达平衡时,A的体积为1.4L。下列说法错误的是( )
2Z(g)+W(g) ΔH <0,达平衡时,A的体积为1.4L。下列说法错误的是( )
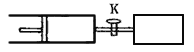
A. 两容器中的反应分别达到平衡时,反应物X的速率:v(B)>v(A)
B. A容器中X的转化率为80%
C. 平衡时两容器的压强:PA<PB
D. 平衡时Y的体积分数:A>B
【答案】D
【解析】A.对X(g)+Y(g)![]() 2Z(g)+W(g)来说,开始时只加入反应物X和Y,该反应将向正反应方向进行以建立化学平衡。对容器A来说,在建立化学平衡的过程中,反应混合物的总物质的量会增大,根据阿伏加德罗定律(同温同容时,压强之比等于物质的量之比),其体积要增大,各组分的物质的量浓度就要减小,其反应速率也要减小。对于B容器来说,体积不变,压强增大,每个时刻的反应速率都将大于A容器,即反应速率:v(B)>v(A),A正确;B.根据阿伏加德罗定律(同温同容时,压强之比等于物质的量之比),达平衡后,混合气体的物质的量是初始时物质的量的1.4倍,即1.4×2mol=2.8mol,即增加了0.8mol,根据化学方程式的计算可知,
2Z(g)+W(g)来说,开始时只加入反应物X和Y,该反应将向正反应方向进行以建立化学平衡。对容器A来说,在建立化学平衡的过程中,反应混合物的总物质的量会增大,根据阿伏加德罗定律(同温同容时,压强之比等于物质的量之比),其体积要增大,各组分的物质的量浓度就要减小,其反应速率也要减小。对于B容器来说,体积不变,压强增大,每个时刻的反应速率都将大于A容器,即反应速率:v(B)>v(A),A正确;B.根据阿伏加德罗定律(同温同容时,压强之比等于物质的量之比),达平衡后,混合气体的物质的量是初始时物质的量的1.4倍,即1.4×2mol=2.8mol,即增加了0.8mol,根据化学方程式的计算可知,
X(g)+Y(g)![]() 2Z(g)+W(g) △n
2Z(g)+W(g) △n
1 1
0.8mol 0.8mol
即达平衡后,反应掉0.8mol,A容器中X的转化率为80%,B正确;C.根据选项A中分析可知平衡时两容器的压强:PA<PB,C正确;D.压强越大越不利于平衡向正反应方向进行,反应物的转化率越小,根据以上分析可知A中反应物的转化率大于B中反应物的转化率,则平衡时Y体积分数A<B,D错误;答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】下表是某些化学键的键能,则生成2mol H2O时,放出的能量为( )
化学键 | H-H | O=O | H-O |
键能(KJ/mol) | 436 | 496 | 463 |
A. 242KJ B. 442 KJ C. 484 KJ D. 448KJ