题目内容
【题目】利用废蚀刻液(含FeCl2、CuCl2及FeCl3)制备碱性蚀刻液[Cu(NH3)4Cl2溶液]和FeCl3·6H2O的主要步骤:用H2O2氧化废蚀刻液,制备氨气,制备碱性蚀刻液[CuCl2+4NH3=Cu(NH3)4Cl2]、固液分离,用盐酸溶解沉淀并制备FeCl3·6H2O。下列实验原理和装置不能达到实验目的的是
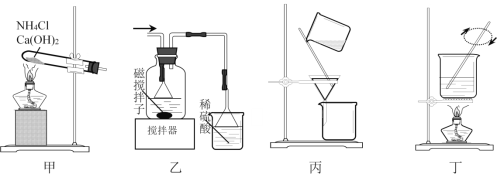
A. 用装置甲制备NH3
B. 用装置乙制备Cu(NH3)4Cl2并沉铁
C. 用装置丙分离Cu(NH3)4Cl2溶液和Fe(OH)3
D. 用装置丁将FeCl3溶液蒸干制备FeCl3·6H2O
【答案】D
【解析】
本实验是制备Cu(NH3)4Cl2和FeCl3·6H2O,根据步骤,用H2O2先将刻蚀液中的Fe2+氧化成Fe3+,实验室常用Ca(OH)2和NH4Cl制备氨气,将氨气刻蚀液中制备碱性刻蚀液,Fe3+与NH3·H2O生成Fe(OH)3沉淀,然后过滤,用盐酸溶解氢氧化铁沉淀,最后蒸发浓缩、冷却结晶得到FeCl3·6H2O;
本实验是制备Cu(NH3)4Cl2和FeCl3·6H2O,根据步骤,用H2O2先将刻蚀液中的Fe2+氧化成Fe3+,实验室常用Ca(OH)2和NH4Cl制备氨气,将氨气刻蚀液中制备碱性刻蚀液,Fe3+与NH3·H2O生成Fe(OH)3沉淀,然后过滤,用盐酸溶解氢氧化铁沉淀,最后蒸发浓缩、冷却结晶得到FeCl3·6H2O;
A、实验室用Ca(OH)2和NH4Cl共热制备氨气,利用甲装置能够制备NH3,甲装置能达到实验目的,故A不符合题意;
B、乙装置制备碱性刻蚀液Cu(NH3)4Cl2,然后Fe3+与氨水反应生成Fe(OH)3,乙装置能完成实验目的,故B不符合题意;
C、丙装置分离固液,丙装置能够达到实验目的,故C不符合题意;
D、FeCl3溶液制备FeCl3·6H2O,采用蒸发浓缩、冷却结晶,不能蒸干,丁装置不能完成实验目的,故D符合题意;

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案