题目内容
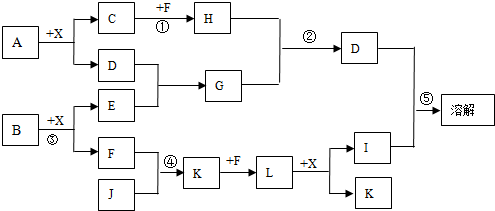
某已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为25%,B的焰色反应呈黄色,C、J、X是同周期的元素的简单氢化物,X为无色液体,C、J为气体,D是一种不溶于水的白色固体。反应生成的水均已略去。它们有如下图所示的关系。

(1)写出化学式:A???????? ,E??????????? ,L?????????? ;
(2)在反应①②③④⑤中属于氧化还原反应的是???????????????????????????? ;
(3)反应③化学方程式为:?????????????????????????????????????????????? ;
(4)写出下列离子方程式:反应②???????????????????????????????????????? ;
G溶液与M溶液的反应?????????????????????????????? ?????????????? 。
(1)Al4C3;NaOH;NO2? (各2分,共6分)(2)①③④(3分)
(3)2Na2O2+2H2O=4NaOH+O2↑ (2分)(4)2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(2分)
(或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-); Al3++3AlO2-+6H2O = 4Al(OH)3↓(2分)
【解析】
试题分析:X为无色液体,推断X为H2O;B的焰色反应为黄色,则B中含有钠元素。由于B与水反应生成两种物质,则B应该是过氧化钠,E和F为氢氧化钠和氧气。C、J、X是同周期的元素的简单氢化物,C、J为气体,且F与J反应,因此F是氧气,则E是氢氧化钠。D是一种不溶于水的白色固体能与氢氧化钠反应,因此D是氧化铝或氢氧化铝。D与E反应生成G,而G与H反应又生成D,所以D应该是氢氧化铝,G是偏铝酸钠。C与氧气的反应物H能与偏铝酸钠反应生成氢氧化铝,因此H可能是CO2,所以C是甲烷,A为碳与铝的化合物,结合给出的质量分数,A为Al4C3,它与水发生水解反应Al4C3+12H2O=4Al(OH)3+3CH4↑;C、J、X是同周期的元素的简单氢化物,C、J为气体,且J与氧气也反应,所以J是氨气,与氧气反应生成NO和水,则K是NO,NO与氧气反应生成NO2,所以L是NO2,二氧化氮溶于水生成NO和硝酸,因此I是硝酸。硝酸与氢氧化铝反应生成硝酸铝和水,即M是硝酸铝,硝酸铝与偏铝酸钠反应又产生氢氧化铝沉淀。
(1)根据以上分析可知A、E、L的化学式分别为Al4C3;NaOH;NO2 ;
(2)有元素化合价升降的反应是氧化还原反应,因此在反应①②③④⑤中属于氧化还原反应的是①③④;
(3)反应③化学方程式为2Na2O2+2H2O=4NaOH+O2↑;
(4)反应②的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(或AlO2-+CO2+2H2O=2Al(OH)3↓+HCO3-);G溶液与M溶液的反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓。
考点:考查无机物推断

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案