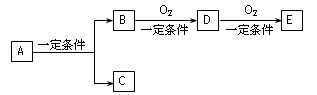
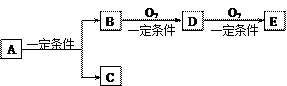题目内容
[化学—选修物质结构与性质](15分)
主要元素W、X、Y、Z的原子序数一次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,他们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为 ,W3分子的空间构型为 ;
(2)X单质与水发生主要反应的化学方程式为 ;
(3)化合物M的化学式为 ,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是 。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有 ,O—C—O的键角约为 ;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z= ;
(5)含有元素Z的盐的焰色反应为 色。许多金属盐都可以发生焰色反应,其原因是 。
主要元素W、X、Y、Z的原子序数一次增大,W的原子最外层电子数是次外层电子数的3倍。X、Y和Z分属不同的周期,他们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
(1)W元素原子的L层电子排布式为 ,W3分子的空间构型为 ;
(2)X单质与水发生主要反应的化学方程式为 ;
(3)化合物M的化学式为 ,其晶体结构与NaCl相同,而熔点高于NaCl。M熔点较高的原因是 。将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中,碳原子采用的杂化方式有 ,O—C—O的键角约为 ;
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z= ;
(5)含有元素Z的盐的焰色反应为 色。许多金属盐都可以发生焰色反应,其原因是 。
(1)2s22p4 V形
(2) 2F2 +2 H2O ="4" HF+ O2
(3)MgO 晶格能大 sp3、sp2 120°
(4)3:1:1
(5)紫 激发态电子从能量高的轨道跃迁到能量低的轨道时,以一定波长(可见光区域)光的形式释放能量。
(2) 2F2 +2 H2O ="4" HF+ O2
(3)MgO 晶格能大 sp3、sp2 120°
(4)3:1:1
(5)紫 激发态电子从能量高的轨道跃迁到能量低的轨道时,以一定波长(可见光区域)光的形式释放能量。
本题主要结合元素推断考查物质结构与性质等知识的综合应用。由W原子最外层电子数是次外层的3倍,可确定W是O元素,结合X、Y、Z分别在不同周期、原子序数关系和题中信息可确定三者分别为F、Mg和K。(1)O原子L层排有6个电子,其排布式为2s22p4,由价层电子对互斥模型可确定O3是V形结构。MgO的熔点之所以高于NaCl,是因为其晶格能较大的缘故。碳酸二甲酯(CH3OCOOCH3)两端碳原子采取sp3杂化,中间碳原子采取sp2杂化,且O—C—O的键角为120°。利用均摊法可以算出立方晶体结构中X:Y:Z=1/4×12:1/8×8:1=3:1:1。
方法提炼:可以借助题中信息推断各元素,如根据(5)中Z有焰色,且原子序数最大,可联想Z为K,则X、Y分别为第二、三周期元素,即X只能为F,根据三者原子序数之和为40,可确定Y为Mg,将这些元素代入题中检验,符合题意。据此可以分析作答。
方法提炼:可以借助题中信息推断各元素,如根据(5)中Z有焰色,且原子序数最大,可联想Z为K,则X、Y分别为第二、三周期元素,即X只能为F,根据三者原子序数之和为40,可确定Y为Mg,将这些元素代入题中检验,符合题意。据此可以分析作答。

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目

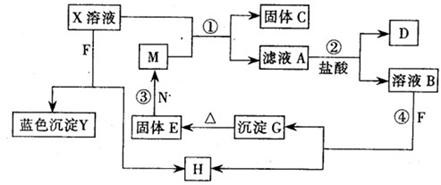

 学方程式是 。A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是 。
学方程式是 。A与盐B的溶液反应时只生成气体C、碳酸钙沉淀和水,则B的化学式是 。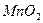 ,反应的化学方程式为 。
,反应的化学方程式为 。