��Ŀ����
������M��һ�ֹ��¿�ʴ����������ӡˢ��·�ͼ��ɵ�·�����У���ϳ�·�����£�
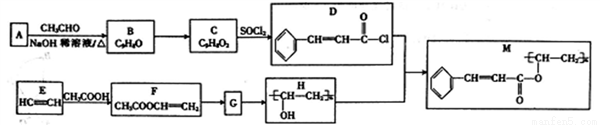
��֪��I. 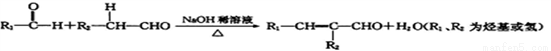
II.�ǻ�ֱ��������̼̼˫����̼ԭ���ϵ��л����Dz��ȶ��ġ�
�ش��������⣺
(1)���й���M��˵����ȷ����______������ĸ����
a.M���ڸ߷��ӻ�����
b.M�ڼ�����Һ�����ȶ�����
c.M��ʹ���Ը��������Һ��ɫ
d.1molM������������Ӧʱ���������4molH2
(2)C�й����ŵ�����Ϊ______����E����F�ķ�Ӧ����Ϊ_________��
(3)F�Ļ�ѧ����Ϊ_______����F����G�Ļ�ѧ����ʽΪ____________��
(4)��ȡ�������廯����W��ֻ�����������������Ļ����Ҳ�����C=C=C���ṹ����D��ͬ���칹�壬W�������Ȼ�����Һ������ɫ��Ӧ����W�Ľṹ����____�֣����������칹�������к˴Ź�������Ϊ�����Ľṹ��ʽΪ____________��
(5)���������ϳ�·�ߣ����һ����HC��CHΪԭ�ϣ��������Լ���ѡ���Ʊ�G�ĺϳ�·�ߣ�________________________��
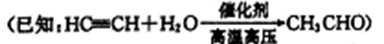
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д������£���һԪ��HA����Һ��KOH��Һ��������(��������仯)��ʵ���������±���
ʵ���� | ��ʼŨ��/mol��L-1 | ��Ӧ����Һ��PH | |
c(HA) | c(KOH) | ||
�� | 0.1 | 0.1 | 9 |
�� | X | 0.2 | 7 |
�����жϲ���ȷ����
A. ʵ��ٷ�Ӧ�����Һ�У�c(K+)>c(A-)>c(OH-)>c(H+)
B. ʵ��ٷ�Ӧ�����Һ�У�c(OH-)= c(K+)-c(A_)=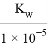 mol��L-1
mol��L-1
C. ʵ��ڷ�Ӧ�����Һ�У�c(A-)+c(HA)>0.1mol��L-1
D. ʵ��ڷ�Ӧ�����Һ�У�c(K+)=c(A-)> c(OH-)=c(H+)


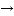 Si B. CO2
Si B. CO2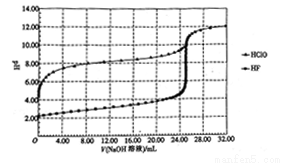
 ������Ҫ�Ļ���ԭ�ϣ���һ�ֺϳ�·�����£�
������Ҫ�Ļ���ԭ�ϣ���һ�ֺϳ�·�����£�
 NH4HCO3(aq) ��H1
NH4HCO3(aq) ��H1  CH4(g)+2H2O(g)����֪��H2������������¶ȵ����߶����ӡ�
CH4(g)+2H2O(g)����֪��H2������������¶ȵ����߶����ӡ�
