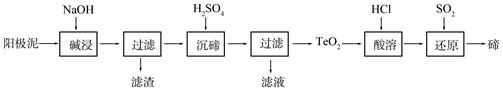
��Ŀ����
������һ��ǿ������������������������ȡ�
(1)O3��KI��Һ��Ӧ���ɵ����ֵ�����________��________(�����ʽ)��
(2)O3��ˮ���ֽ⣬һ�������£�O3��Ũ�ȼ���һ�������ʱ��(t)���±���ʾ����֪��O3����ʼŨ��Ϊ0.0216 mol/L��
��pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���________��
����30�桢pH��4.0�����£�O3�ķֽ�����Ϊ________mol/(L��min)��
�۾ݱ��еĵݱ���ɣ��Ʋ�O3�����������·ֽ��������������˳��Ϊ________(����ĸ����)��
a��40�桢pH��3.0������ b��10�桢pH��4.0
c��30�桢pH��7.0
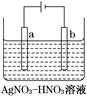
(3)O3���ɳ���������(ԭ����ͼ)���ϡ�����Ƶá�
��ͼ������Ϊ________(�A����B��)����缫��ӦʽΪ_______________________��
����C��ͨ��O2����A���ĵ缫��ӦʽΪ________��
����C����ͨ��O2��D��E���ֱ��ռ���x L��y L����(��״��)����E���ռ���������O3��ռ���������Ϊ________(����O3�ķֽ�)��
(1)I2��O2
(2)��OH������1.00��10��4����b��a��c
(3)��A��2H����2e��=H2��
��O2��4H����4e��=2H2O����(x��2y)/y
����

��֪I����Fe2+��SO2��Cl����H2O2���л�ԭ�ԣ�������������Һ�л�ԭ�Ե�ǿ��˳��ΪCl��< Fe2+< H2O2< I��< SO2�������з�Ӧ���ܷ�������
| A��2Fe3++SO2+2H2O=2Fe2++SO42��+4H+ |
| B��Cl2+SO2+2H2O=H2SO4+2HCl |
| C��H2O2+2H++ SO42��=SO2��+O2��+2H2O |
| D��2I2+H2O2=2H2O+O2��+4 I�� |
���������ʡ���������ƵƵ������Ϊ��ֹ�ڴ���֮���߲����У�������Ҫ�����ĸ�����������Ư���ȡ�
(1)����������Ŀǰ�����Ϲ��ϵĵ��Ĵ���Ч�����Ĺ�����������������KClO3��SO2��H2SO4�����·�Ӧ�Ƶá���д����Ӧ�����ӷ���ʽ�� ��
(2)��̼������һ������̬Ư������ѧʽ�ɱ�ʾΪNa2CO3��3H2O2��������Na2CO3��H2O2��˫�����ʡ���̼�������������ʾ��ᷢ����ѧ��Ӧ��ʧЧ�����й�̼����ֻ������������Ӧ���� ��
| A��MnO2 | B��KMnO4��Һ | C��ϡ���� | D��Na2SO3��Һ |
 ��1�����յĹ����в��õ��ǡ��������ա��Ĵ�ʩ����ô�ʩ���ŵ��ǣ���_______________
��1�����յĹ����в��õ��ǡ��������ա��Ĵ�ʩ����ô�ʩ���ŵ��ǣ���_______________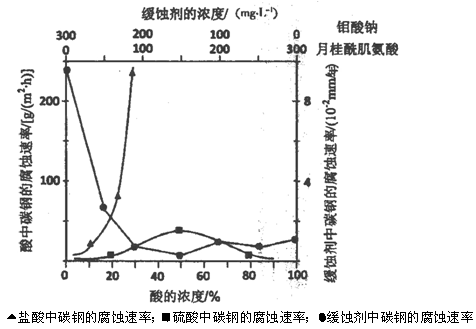
 Lix(MoS2)n�����طŵ�ʱ��������Ӧʽ�ǣ�___________________________________��
Lix(MoS2)n�����طŵ�ʱ��������Ӧʽ�ǣ�___________________________________��