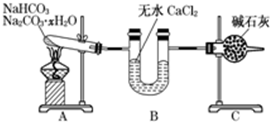
题目内容
16.某金属M2+的第三层中有15个电子,该金属名称是( )| A. | Fe | B. | Mn | C. | Co | D. | Ni |
分析 某金属M2+的第三层中有15个电子,根据电子排布规律知,该离子K、L层分别排有2、8个电子,M原子失去2个电子生成M2+,则M原子核外电子数为2+8+15+2=27,为第四周期第VIII族元素.
解答 解:某金属M2+的第三层中有15个电子,根据电子排布规律知,该离子K、L层分别排有2、8个电子,M原子失去2个电子生成M2+,则M原子核外电子数为2+8+15+2=27,为第四周期第VIII族元素Co,故选C.
点评 本题考查原子核外电子排布,为高频考点,明确原子核外电子排布规律及原子失电子规律是解本题关键,熟记前36号元素在周期表中的位置,题目难度不大.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
7.不是构成原电池必需具备的条件是( )
| A. | 活泼性不同的两极 | B. | 闭合回路 | ||
| C. | 电源 | D. | 电解质溶液 |
11.将由4.2g碳酸氢钠固体与5.8g氢氧化钠固体组成的混合物物在试管中加热,产生的气体通入澄清石灰水中,直至试管中固体质量不再变化得到固体A,则下列说法正确的是( )
| A. | 固体A中只含有氢氧化钠 | B. | 固体A中含有碳酸氢钠 | ||
| C. | 固体A中只含有碳酸钠 | D. | 固体A的质量为9.1g |
4.下列物质的化学式与名称、分类完全相符的是( )
| A. | 酒精、CH3OH、有机物 | B. | 硝酸钠、NaNO3、盐 | ||
| C. | 氧化铁、Fe3O4、氧化物 | D. | 纯碱,NaOH、碱 |

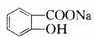 B
B D
D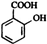 .写出D→E的反应的化学方程式
.写出D→E的反应的化学方程式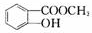 +H2O.
+H2O.