题目内容
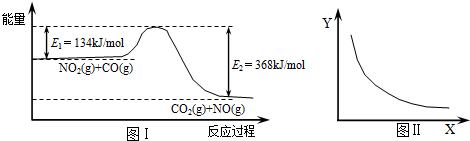
(2009?南京二模)图Ⅰ是NO2(g)+CO(g)?CO2(g)+NO(g)反应过程中能量示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ.
下列有关说法正确的是( )

下列有关说法正确的是( )
分析:A、反应的焓变=拆化学键吸收能量-形成化学键放出能量;
B、起始浓度增大,反应物的转化率不一定减小;
C、反应是放热反应,温度升高反应逆向进行;
D、反应前后气体体积不变,气体形成的化学平衡质量守恒;
B、起始浓度增大,反应物的转化率不一定减小;
C、反应是放热反应,温度升高反应逆向进行;
D、反应前后气体体积不变,气体形成的化学平衡质量守恒;
解答:解:A、反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234kJ/mol,故A正确;
B、两种反应物的化学平衡,增加一种物质的量,会提高另一种转化率,故B错误;
C、该反应是放热反应,升温,化学平衡逆向进行,二氧化碳浓度减小,故C正确;
D、气体形成的平衡体系中气体质量不变,反应前后体积不变,所以密度不变,故D错误;
故选AC.
B、两种反应物的化学平衡,增加一种物质的量,会提高另一种转化率,故B错误;
C、该反应是放热反应,升温,化学平衡逆向进行,二氧化碳浓度减小,故C正确;
D、气体形成的平衡体系中气体质量不变,反应前后体积不变,所以密度不变,故D错误;
故选AC.
点评:本题考查了反应焓变的含义和计算,化学平衡的影响因素,反应物的转化率变化,主要是理解图象分析方法.

练习册系列答案
相关题目
 下列说法错误的是( )
下列说法错误的是( )