题目内容
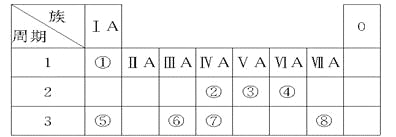
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1) 由②和④组成,造成温室效应的气体的结构式是________
(2) ①、④、⑤、⑧中的某些元素可形成多种既含离子键又含共价键的化合物,写出其中一种化合物的电子式: 。
(3) ④、⑤、⑥的原子半径由大到小的顺序为(填元素符号) 。
(4) ②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式) 。
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为_____________________
【答案】(1)O==C==O
(2)![]() 或过氧化钠的电子式
或过氧化钠的电子式
(3)Na>Al>O
(4)HNO3>H2CO3>H2SiO3(或H4SiO4)
(5)2Al+2OH-+2H2O===2AlO+3H2↑
【解析】试题分析:根据元素周期表①②③④⑤⑥⑦⑧分别是H、C、N、O、Na、Al、Si、Cl元素。
(1) 由②和④组成,造成温室效应的气体是二氧化碳,结构式是O==C==O
(2) ①、④、⑤、⑧中的某些元素可形成多种既含离子键又含共价键的化合物,是次氯酸钠、氢氧化钠或过氧化钠等,电子式:![]() 。
。
(3) 电子层数越多半径越大;电子层数相同,质子数越多半径越小,④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O。
(4) ②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3。
(5)铝与氢氧化钠反应的离子方程式为2Al+2OH-+2H2O===2AlO+3H2↑。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目