题目内容
11. 实验室可以用二氧化锰和浓盐酸在加热条件下制备氯气.下图为
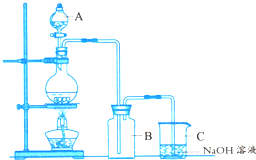
实验室可以用二氧化锰和浓盐酸在加热条件下制备氯气.下图为实验室制取氯气的装置.请回答下列问题:
(1)仪器A 的名称为分液漏斗
(2)装置C中氯气与NaOH溶液反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O;
(3)将湿润的蓝色石蕊试纸放入充满氯气的装置B中,观察到的现象是试纸先变红,后褪色.
分析 (1)熟悉仪器形状,说出其名称;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(3)氯气与水反应生成盐酸与次氯酸,盐酸具有酸性,次氯酸具有漂白性.
解答 解:(1)图中仪器A为分液漏斗;
故答案为:分液漏斗;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(3)氯气与水反应生成盐酸与次氯酸,盐酸具有酸性,次氯酸具有漂白性,将湿润的蓝色石蕊试纸放入充满氯气的装置B中,现象为:试纸先变红,后褪色;
故答案为:试纸先变红,后褪色.
点评 本题考查了氯气的实验室制备和性质的检验,熟悉制备原理和氯气性质是解题关键,题目难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
2.下列对NaCl的分类正确的是( )
| A. | 混合物 | B. | 化合物 | C. | 氧化物 | D. | 有机物 |
19.下列离子方程式书写正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| B. | 碳酸氢钠溶液与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 铝与氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 铁与氯化铁溶液反应:Fe3+Fe═2Fe2+ |
6.下列说法正确的是( )
| A. | 华北地区水资源十分匮乏,必须节约用水 | |
| B. | 明矾能沉降水中的悬浮物,又能杀菌消毒 | |
| C. | 活性炭既可以吸附水中的异味,又可以降低水的硬度 | |
| D. | 长期饮用纯净水,不利于人体健康 |
16.NA代表阿伏加德罗常数,下列说法中,正确的是( )
| A. | 在同温同压时,相同体积的任何气体单质所含的原子数目相同 | |
| B. | 标准状况下,22.4 L水所含的水分子数为NA | |
| C. | 在常温常压下,11.2 L氮气所含的原子数目为NA | |
| D. | 34g氨气所含质子数目为20 NA |
1.下列叙述中正确的是( )
| A. | 在稀溶液中1mol酸和1mol碱完全反应所放出的热量,叫做中和热 | |
| B. | 在101kP时1mol物质燃烧时所放出的热量叫做该物质的燃烧热 | |
| C. | 热化学方程式中,各物质前的化学计量数不表示分子个数 | |
| D. | 在相同条件下,1 molH20(l)完全分解吸收的热量与H2、O2化合生成1 molH2O(g)放出的热量数值相等 |
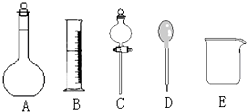 我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸(密度为1.19g/cm3)配制成240mL 0.1mol•L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸(密度为1.19g/cm3)配制成240mL 0.1mol•L-1的盐酸溶液.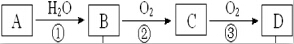 已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.现以A为主要原料合成乙酸,其合成路线如图所示.
已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.现以A为主要原料合成乙酸,其合成路线如图所示.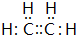
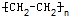 .
.