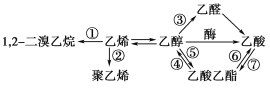
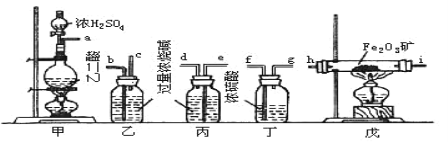
题目内容
【题目】针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的( )
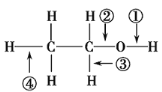
A. 与金属钠反应时,①键断裂
B. 与浓硫酸共热至170℃时,②、④键断裂
C. 在Ag催化下与O2反应时,①、③键断裂
D. 与醋酸、浓硫酸共热时,②键断裂
【答案】D
【解析】
A.与金属钠反应时,断裂羟基中的O-H键,即①键断裂,A正确;
B.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,断裂C-O键与甲基中1个C-H键,即②、④键断裂,B正确;
C.在Ag催化下与O2反应,发生催化氧化生成乙醛,断裂羟基中O-H键和羟基碳上的一个C-H键,即①、③键断裂,C正确;
D.与醋酸、浓硫酸共热时,乙醇分子中羟基上O-H键断裂,即①键断裂,D错误;
故合理说法是D。

 阅读快车系列答案
阅读快车系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | ||||||||||||||||
[ | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o |
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为_________。
(2)画出d元素原子的结构示意图_______________________________,其气态氢化物溶于水显_____________性。(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱________>__________。
(4)表中j元素在元素周期表中的位置是______________________。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是___________(填写化合物的化学式,下同),具有两性的是_____________,
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如图。
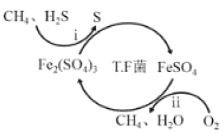
过程i的离子反应方程式为_____。
已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
Fe2+的氧化速率 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在表中选择最佳pH范围是____<pH<____,这样选择的原因是:______。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
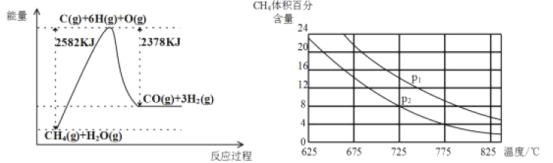
(3)①该过程的热化学方程式是_____。
②比较压强P1和P2的大小关系:P1____P2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程如示意图如图。
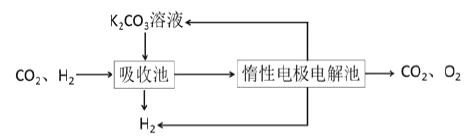
(4)吸收池中发生反应的离子方程式是______。