题目内容
【题目】将30mL 0.5molL-1 NaOH溶液加水稀释到500mL,稀释后的溶液中NaOH的物质的量浓度为
A. 0.3 molL-1 B. 0.05 molL-1 C. 0.03 molL-1 D. 0.02 molL-1
【答案】C
【解析】
根据稀释前后溶质的物质的量不变进行计算,c1V1=c2V2,可以计算稀释后物质的量浓度。
稀释前,NaOH溶液体积为30mL、浓度为0.5molL-1,稀释后溶液体积为500mL,列式可得30mL ×0.5molL-1=c2×500mL,所以c2=0.03 molL-1。答案为C。

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案【题目】碳酸锂广泛应用于化工、冶金等行业。工业上利用锂辉石(Li2Al2Si4Ox)制备碳酸锂的流程如下:
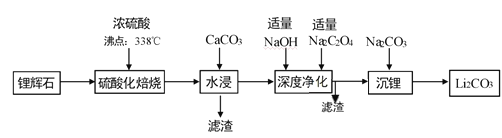
已知:①CaC2O4难溶于水;②Li2CO3的溶解度(g/L)。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
请回答下列问题:
(1)锂辉石(Li2Al2Si4Ox)可以用氧化物的形式表示其组成,形式为___________。
(2)“深度净化”时,加入适量Na2C2O4的目的是__________________。
(3)“沉锂”需要在95℃以上进行,主要原因是_____________________。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH 溶液做阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是__________________,宜选用_________(“阳”或“阴”)离子交换膜。
②b中,生成Li2CO3反应的化学方程式是________________________。