��Ŀ����
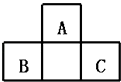
����Ŀ����ͼA��B��C��ij����С����Ƶ���ȡ������������Ȫʵ�������װ��ʾ��ͼ����ȡNH3ѡ���Լ���ͼ��ʾ���ش��������⣺
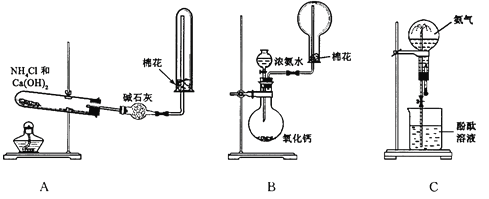
��1����Aͼ��ʾ��װ�ÿ��Ʊ������NH3
�ٷ�Ӧ�Ļ�ѧ����ʽΪ��________________________________________��װ�����ռ�NH3���Թܿڷ������ŵ�������_________________________________________��
�ڸ�����и�����ܷ������ˮCaCl2___________��������_______________________��
��2����Bͼ��ʾ��װ�ÿɿ�����ȡ�ϴ���NH3������Ȫʵ�顣����Bͼ��ʾ��װ�ü��Լ��ش��������⣺
���û�ѧ����ʽ��ʾŨ��ˮ����CaO���д���NH3�ݳ��Ĺ��̣�_________________________
�ڼ���NH3�Ƿ��ռ�����ʵ�鷽���ǣ�______________________________________________��
��3����Cͼ��ʾ��װ�ý�����Ȫʵ�飬�ϲ���ƿ�ѳ������ﰱ����������Ȫ�IJ�����___________________________����ʵ���������Һ����������ƿ����ˮ��Ũ��Ϊ_______________________������ʵ���ڱ���½��У��������Cװ����ƿ��NH3����������ͬ״������ͬ���H2������10��������Ȫʵ����Ϻ���ƿ��ˮ����������ƿ�ݻ���___________(�����֮����)��
���𰸡� 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O ��ֹ����������ʹNH3�����Թ� ���� CaCl2+8NH3��CaCl2��8NH3 CaO+H2O��Ca(OH)2��Ӧ����NH3��H2O
CaCl2+2NH3��+2H2O ��ֹ����������ʹNH3�����Թ� ���� CaCl2+8NH3��CaCl2��8NH3 CaO+H2O��Ca(OH)2��Ӧ����NH3��H2O![]() NH3��+H2O �ò�����պȡ����Ũ������ռ�NH3���Թܿڣ����������̣�˵���Թ����ռ���NH3����֮����û���ռ��� ����ʪ��ĺ�ɫʯ����ֽ�����ռ�NH3���Թܿڣ���ʪ��ĺ�ɫʯ����ֽ��������˵��NH3���ռ�������֮����û���ռ��� ��ֹˮ�м�����ͷ�ι��е�ˮ 1/22.4 mol/L
NH3��+H2O �ò�����պȡ����Ũ������ռ�NH3���Թܿڣ����������̣�˵���Թ����ռ���NH3����֮����û���ռ��� ����ʪ��ĺ�ɫʯ����ֽ�����ռ�NH3���Թܿڣ���ʪ��ĺ�ɫʯ����ֽ��������˵��NH3���ռ�������֮����û���ռ��� ��ֹˮ�м�����ͷ�ι��е�ˮ 1/22.4 mol/L ![]()
����������1�����ڼ��������£��Ȼ�狀��������Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͱ�����2NH4Cl+Ca(OH)2![]() CaCl2+2NH3��+2H2O�����������壬���Ϳ��������������������������Ƿ�ֹ����������ʹNH3�����Թܣ����Ȼ�狀Ͱ����ܷ�����ӦCaCl2+8NH3=CaCl28NH3�����Ը�����и�������ܸ�����ˮCaCl2����2���������ƺ�ˮ��Ӧ�����������ƣ��ҷų����������������ƺ�ˮ�ų��������ܴٽ���ˮ�ķֽ⣺NH3��H2O
CaCl2+2NH3��+2H2O�����������壬���Ϳ��������������������������Ƿ�ֹ����������ʹNH3�����Թܣ����Ȼ�狀Ͱ����ܷ�����ӦCaCl2+8NH3=CaCl28NH3�����Ը�����и�������ܸ�����ˮCaCl2����2���������ƺ�ˮ��Ӧ�����������ƣ��ҷų����������������ƺ�ˮ�ų��������ܴٽ���ˮ�ķֽ⣺NH3��H2O![]() NH3��+H2O���ڰ�����ʹʪ��ĺ�ɫʯ����ֽ�������������Ȼ��ⷴӦ���ɰ��̣����Կ����Ȼ����ʪ��ĺ�ɫʯ����ֽ���飬���ò�����պȡ����Ũ������ռ�NH3���Թܿڣ����������̣�˵���Թ����ռ���NH3����֮����û���ռ���������ʪ��ĺ�ɫʯ����ֽ�����ռ�NH3���Թܿڣ���ʪ��ĺ�ɫʯ����ֽ��������˵��NH3���ռ�������֮����û���ռ�������3��NH3�����ܽ���ˮ����ֹˮ�м�����ͷ�ι��е�ˮ�����ڰ���Ѹ���ܽ����ƿ������ѹǿѸ�ټ�С��������Һ������ƿ������Ȫ�������ڳ�����Һ����ˮ��Ũ����
NH3��+H2O���ڰ�����ʹʪ��ĺ�ɫʯ����ֽ�������������Ȼ��ⷴӦ���ɰ��̣����Կ����Ȼ����ʪ��ĺ�ɫʯ����ֽ���飬���ò�����պȡ����Ũ������ռ�NH3���Թܿڣ����������̣�˵���Թ����ռ���NH3����֮����û���ռ���������ʪ��ĺ�ɫʯ����ֽ�����ռ�NH3���Թܿڣ���ʪ��ĺ�ɫʯ����ֽ��������˵��NH3���ռ�������֮����û���ռ�������3��NH3�����ܽ���ˮ����ֹˮ�м�����ͷ�ι��е�ˮ�����ڰ���Ѹ���ܽ����ƿ������ѹǿѸ�ټ�С��������Һ������ƿ������Ȫ�������ڳ�����Һ����ˮ��Ũ����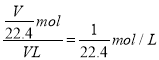 ����ƿ��NH3����������ͬ״������ͬ���H2������10����������ƿ�������ƽ����������������10��������ƿ�������ƽ����������20������ʮ�ֽ��淨
����ƿ��NH3����������ͬ״������ͬ���H2������10����������ƿ�������ƽ����������������10��������ƿ�������ƽ����������20������ʮ�ֽ��淨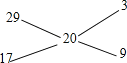 ��֪�����Ͱ��������֮��Ϊ1��3������Ȫʵ����Ϻ���ƿ��ˮ����������ƿ�ݻ���3/4��
��֪�����Ͱ��������֮��Ϊ1��3������Ȫʵ����Ϻ���ƿ��ˮ����������ƿ�ݻ���3/4��

����Ŀ�����������Ҫ�ɷֿɱ�ʾΪFeOCr2O3 �� ������MgO��Al2O3��Fe2O3�����ʣ��������Ը�����Ϊԭ���Ʊ��ظ���أ�K2Cr2O7��������ͼ��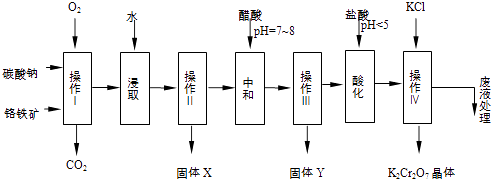
��֪��
��4FeOCr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2����
8Na2CrO4+2Fe2O3+8CO2����
��Na2CO3+Al2O3 ![]() 2NaAlO2+CO2����
2NaAlO2+CO2����
��������ش��������⣺
��1������I�ڳ����¸÷�Ӧ�ٶȼ��������д�ʩ����ʹ��Ӧ����������� ��
A.�����¶�
B.ͨ������Ŀ���
C.��ԭ�Ϸ���
D.���Ӵ��������
��2������X����Ҫ��������д��ѧʽ����
��3���ữ���������������ҺpH��5���������Ŀ���� �� �����ӷ���ʽ��ʾ��
��4������ iv�жಽ��ɣ����K2Cr2O7����IJ��������ǣ�����KCl���塢����Ũ��������ϴ�ӡ����
��5������������ʵ��ܽ�����ݣ�����������Ӧ�Ļ�ѧ����ʽ�ǣ�Na2Cr2O7+2KCl��K2Cr2O7��+2NaCl���÷�Ӧ����Һ���ܷ����������� �� ������˵����
���� | �ܽ��/��g/100gˮ�� | ||
0��C | 40��C | 80��C | |
KCl | 28 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38 |
K2Cr2O7 | 4.7 | 26.3 | 73 |
Na2Cr2O7 | 163 | 215 | 376 |
��6������ƷY��Ҫ��������������������þ���������ܻ����P���������ʣ���ȷ����Y���������������ķ����dz�ȡn g��Ʒ�������������д�Լ������ܽ⡢���ˡ�������д�Լ����������ա���ȴ���������ø������m g��������Ʒ��������������������Ϊ���ú�m��n�Ĵ���ʽ��ʾ����