题目内容
根据主族元素的原子序数不能确定的是( )
| A、质子数 | B、中子数 |
| C、价电子数 | D、周期,族数 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:元素周期表中,原子序数=质子数=核电荷数=核外电子数;中子数=质量数-质子数,以此解答该题.
解答:
解:A.质子数等于元素原子序数,故A不选;
B.根据原子序数无法确定质量数,无法确定中子数,故B选;
C.电中性原子原子序数=质子数=核外电子数,结合核外电子排布规律,可以确定每层电子数,故C不选;
D.由原子序数可确定核外电子排布,由周期数等于电子层数,主族数等于最外层电子数可知,可确定元素在周期表中的位置,故D不选.
故选B.
B.根据原子序数无法确定质量数,无法确定中子数,故B选;
C.电中性原子原子序数=质子数=核外电子数,结合核外电子排布规律,可以确定每层电子数,故C不选;
D.由原子序数可确定核外电子排布,由周期数等于电子层数,主族数等于最外层电子数可知,可确定元素在周期表中的位置,故D不选.
故选B.
点评:本题考查原子结构与性质,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大,注意基础知识的掌握.

练习册系列答案
相关题目
已知乙烯为平面结构,因此1,2-二氯乙烯可以形成两种不同的空间异构体: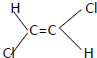 和
和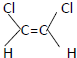 .下列各物质中,能形成类似上述两种空间异构体的是( )
.下列各物质中,能形成类似上述两种空间异构体的是( )
 和
和 .下列各物质中,能形成类似上述两种空间异构体的是( )
.下列各物质中,能形成类似上述两种空间异构体的是( )| A、1,1-二氯乙烯 |
| B、2-甲基-2-戊烯 |
| C、3-甲基-2-戊烯 |
| D、1-戊烯 |
在一定容的密闭容器中,放入3L X(g)和2L Y(g),在一定条件下发生下列反应:4X(g)+3Y(g)?2Q(g)+nR(g).达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,则该化学方程式中的n值是( )
| A、3 | B、4 | C、5 | D、6 |
 某期刊封面上有如下一个常见分子的球棍模型图图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图代表的有机物中含有的官能团是( )
某期刊封面上有如下一个常见分子的球棍模型图图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图代表的有机物中含有的官能团是( )| A、氨基和羧基 |
| B、碳碳双键和羧基 |
| C、碳碳双键和羟基 |
| D、氨基和醛基 |
从硫元素的化合价判断,含硫元素的下列物质只作氧化剂的是( )
| A、Na2S |
| B、S |
| C、SO2 |
| D、H2SO4 |
下列实验操作不正确的是( )
| A、从碘水中提取单质碘,不能用无水乙醇代替CCl4 |
| B、MgCl2溶液混有少量FeCl3,加足量Mg(OH)2调pH后过滤 |
| C、用广泛pH试纸测得0.10mol?L-1 NH4Cl溶液的pH=5.2 |
| D、CO2混有少量SO2,除杂试剂和方法为:酸性KMnO4溶液、浓硫酸,洗气 |
能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是( )
| A、点燃,能燃烧的是矿物油 |
| B、测定沸点,有固定沸点的是矿物油 |
| C、加入水中,浮在水面上的是地沟油 |
| D、加入足量氢氧化钠溶液共热,不分层的是地沟油 |