题目内容
(共8分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)、④、⑤、⑥的原子半径由大到小的顺序为 (填元素符号)。
②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是 (填化学式)。
(2)、①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(3)、由表中两种元素的原子按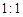 组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。
组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。
a.MnO2 b.Na2SO4 c.Na2SO3 d.CaCO3
(4)、由表中元素形成的物质X、Y、Z、M、N可发生以下反应:
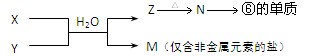
X溶液与Y溶液反应的离子方程式为 ;
常温下,为使0.1 mol/L M溶液中电离出的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至pH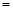 。
。
| | IA | | | | | | | 0 |
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | | ⑦ | | ⑧ | |
(1)、④、⑤、⑥的原子半径由大到小的顺序为 (填元素符号)。
②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是 (填化学式)。
(2)、①、④、⑤、⑧四种元素中,某些元素间可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(3)、由表中两种元素的原子按
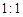 组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。
组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号) 。a.MnO2 b.Na2SO4 c.Na2SO3 d.CaCO3
(4)、由表中元素形成的物质X、Y、Z、M、N可发生以下反应:
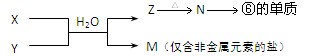
X溶液与Y溶液反应的离子方程式为 ;
常温下,为使0.1 mol/L M溶液中电离出的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至pH
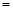 。
。(1). Na>Al>O (1分) HClO4>H3PO4> H2CO3 (1分)
(2).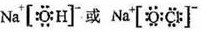 (1分) (3). a (1分)
(1分) (3). a (1分)
(4).Al3++3NH3?H2O→Al(OH)3↓+3NH4+ (2分) pH=7 (2分)
(2).
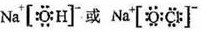 (1分) (3). a (1分)
(1分) (3). a (1分)(4).Al3++3NH3?H2O→Al(OH)3↓+3NH4+ (2分) pH=7 (2分)
根据元素在周期表中的位置可知,①-⑧分别是H、C、N、O、Na、Al、P、Cl。
(1).同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。同主族自上而下,原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。非金属性越强,最高价氧化物的水化物的酸性越强,所以答案是Na>Al>O 、 HClO4>H3PO4> H2CO3。
(2)符合条件的是氢氧化钠或次氯酸钠,电子式分别是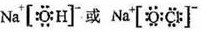
(3)该液态化合物是双氧水,常用二氧化锰作催化剂,答案选a。
(4)M是只含有非金属元素的盐,因此是铵盐。X和Y的反应应该是复分解反应,所以Z是沉淀,即为氢氧化铝,氢氧化铝加热分解得到氧化铝,氧化铝电解得到单质铝。所以X、Y分别是铝盐和氨水。M中NH4+水解显酸性,所以应该加入氨水,才有可能使M溶液中电离出的阴、阳离子浓度相等。根据电荷守恒可知,当pH=7时即可。
(1).同周期自左向右原子半径逐渐减小,金属性逐渐减弱,非金属性逐渐增强。同主族自上而下,原子半径逐渐增大,金属性逐渐增强,非金属性逐渐减弱。非金属性越强,最高价氧化物的水化物的酸性越强,所以答案是Na>Al>O 、 HClO4>H3PO4> H2CO3。
(2)符合条件的是氢氧化钠或次氯酸钠,电子式分别是
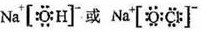
(3)该液态化合物是双氧水,常用二氧化锰作催化剂,答案选a。
(4)M是只含有非金属元素的盐,因此是铵盐。X和Y的反应应该是复分解反应,所以Z是沉淀,即为氢氧化铝,氢氧化铝加热分解得到氧化铝,氧化铝电解得到单质铝。所以X、Y分别是铝盐和氨水。M中NH4+水解显酸性,所以应该加入氨水,才有可能使M溶液中电离出的阴、阳离子浓度相等。根据电荷守恒可知,当pH=7时即可。

练习册系列答案
相关题目
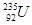 的原子核内的中子数是
的原子核内的中子数是