题目内容
【题目】下图是周期表中短周期的一部分,A、B、C三种元素原子核外的电子数之和等于B原子的质量数。B原子核内的质子数和中子数相等。下列叙述不正确的是
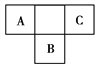
A. 三种元素的原子半径的大小顺序是B>C>A
B. A元素最高价氧化物对应的水化物具有强氧化性
C. B元素的氧化物、氢化物的水溶液都呈酸性
D. C元素是非金属性最强的元素
【答案】A
【解析】令A核外电子数为a,则C的核外电子数为a+2,B的核外电子数为a+9,A、B、C三种元素原子核外的电子数之和等于B原子的质量数,且B原子的质子数等于中子数,即有a+a+2+a+9=2(a+9),解得a=7,即A为N,C为F,B为S,A、同主族从上到下,原子半径增大,同周期从左向右原子半径减小,因此原子半径:S>N>F,故A说法错误;B、A的最高价氧化物对应水化物是HNO3,HNO3是氧化性酸,故B说法正确;C、B的氧化物是SO2、SO3,其水溶液为H2SO3、H2SO4,都显酸性,S的氢化物为H2S,属于二元弱酸,故C说法正确;D、同主族从上到下非金属性减弱,同周期从左到右非金属性增强,因此F的非金属性最强,故D说法正确。

练习册系列答案
相关题目