题目内容
(8分)为除去粗盐中的Ca2+、Mg2+、SO42—以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
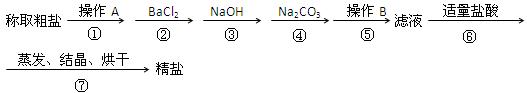
(1)第①步中,操作A是 ,第⑤步中,操作B ;
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
, ;
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。

(1)第①步中,操作A是 ,第⑤步中,操作B ;
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
, ;
(3)若先用盐酸调pH再过滤,将对实验结果产生影响,其原因是
。
(8分)(1)溶解(1分)过滤(1分)(共2分)
(2)CaCl2 + Na2CO3 = CaCO3↓+2NaCl;(2分) BaCl2 + Na2CO3 = BaCO3↓+2NaCl(2分)
(3)操作③④中生成的Mg(OH)2、CaCO3、BaCO3会与盐酸反应,从而影响制 得精盐的纯度(2分)
得精盐的纯度(2分)
(2)CaCl2 + Na2CO3 = CaCO3↓+2NaCl;(2分) BaCl2 + Na2CO3 = BaCO3↓+2NaCl(2分)
(3)操作③④中生成的Mg(OH)2、CaCO3、BaCO3会与盐酸反应,从而影响制
 得精盐的纯度(2分)
得精盐的纯度(2分)略

练习册系列答案
相关题目
 进行了实验现象的假设,请你帮助他对这些假设作一些判断:
进行了实验现象的假设,请你帮助他对这些假设作一些判断:

 析讨论:
析讨论: