题目内容
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.得到的废液中含有Fe2+、Cu2+、Fe3+和Cl﹣.为回收铜并得到纯净的FeCl3溶液,下面是综合利用的主要流程: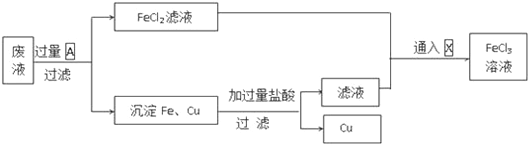
(1)FeCl3溶液和铜反应的离子方程式为__。
(2)上述方框内物质A和X的化学式:A__,X__。上述流程中有关Fe2+和Fe3+相互转化的离子方程式是__、__。
【答案】 2Fe3++Cu=2Fe2++Cu2+ Fe Cl2 2Fe3++Fe=3Fe2+ Cl2+2Fe2+=2 Cl﹣+2Fe3+
【解析】由工艺流程可知,滤渣中含有金属铁和铜,目的是制取氯化铁,废液应该与过量的Fe反应,置换出铜,故A为Fe,得到滤液FeCl2,通入X氯气可以得到氯化铁;滤渣中含有金属Cu、未反应的Fe,需要加入过量盐酸,溶解铁,过滤,回收铜,滤液中含有FeCl2,与FeCl2滤液合并,制备氯化铁溶液。
(1)FeCl3溶液和铜反应生成氯化亚铁和氯化铜,反应的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)上述分析可知A为Fe,X为Cl2,上述流程中有关Fe2+和Fe3+相互转化的离子方程式是2Fe3++Fe=3Fe2+,Cl2+2Fe2+=2 Cl-+2Fe3+,故答案为:Fe;Cl2;2Fe3++Fe=3Fe2+;Cl2+2Fe2+=2Cl-+2Fe3+。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目