题目内容
10.下列离子方程式改写为化学方程式正确的是( )| A. | Cu2++2 OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | H++OH-═H2O CH3COOH+NaOH═CH3COONa+H2O | |
| C. | Ag++Cl-═AgCl↓ AgNO3+HCl═AgCl↓+HNO3 | |
| D. | Ca2++HCO3-+OH-═CaCO3↓+H2O Ca(HCO3)2+Ca(OH)2═2CaCO3↓+2H2O |
分析 A.碳酸铜不能拆开,离子方程式中应该保留化学式;
B.醋酸为弱酸,离子方程式中需要保留分子式;
C.硝酸银和氯化氢都是易溶的强电解质,二者反应生成难溶物氯化银和易溶的强电解质硝酸;
D.碳酸氢钙和氢氧化钙都是易溶的强电解质,二者反应生成碳酸钙沉淀和水.
解答 解:A.CuCO3+2NaOH═Cu(OH)2↓+Na2CO3反应中,CuCO3不能拆开,不能用Cu2++2OH-═Cu(OH)2↓表示,故A错误;
B.CH3COOH+NaOH═CH3COONa+H2O的离子方程式为:CH3COOH+OH-═CH3COO-+H2O,不能用H++OH-═H2O表示,故B错误;
C.AgNO3+HCl═AgCl↓+HNO3的离子方程式为:Ag++Cl-═AgCl↓,故C正确;
D.Ca(HCO3)2+Ca(OH)2═2CaCO3↓+2H2O的离子方程式为:Ca2++HCO3-+OH-═CaCO3↓+H2O,故D正确;
故选CD.
点评 本题考查了离子方程式的书写,为中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等.

练习册系列答案
相关题目
18.下列离子方程式中,正确的是( )
| A. | 稀硫酸与氢氧化钡溶液反应:H++OH-═H2O | |
| B. | 铁与氯化铁溶液反应:Fe+2Fe3+═3Fe2+ | |
| C. | 实验室制氯气:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O | |
| D. | 向氯化铝溶液滴加少量氨水:Al3++3OH-═Al(OH)3↓ |
5.酸雨形成的主要原因是( )
| A. | 工业上大量燃烧含硫燃料 | B. | 自然界中硫化物分解 | ||
| C. | 汽车排出大量尾气 | D. | 可燃冰燃烧 |
15.如图是一种合金材料储氢后的晶胞结构示意图,该晶体中X、Y、Z微粒的个数比为( )
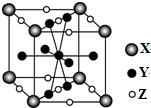

| A. | 1:1:1 | B. | 1:3:3 | C. | 4:4:5 | D. | 1:5:3 |
2.下列说法中正确的是( )
| A. | H2SO4的摩尔质量是98g | |
| B. | 标准状况下,2.24 L水的质量是1.8g | |
| C. | 16gO3比16gO2所含的氧原子数多 | |
| D. | 22g二氧化碳与标准状况下11.2L HCl含有相同的分子数 |
20.下列关于强弱电解质的说法,错误的是( )
| A. | 强电解质在溶液中完全电离,不存在电离平衡 | |
| B. | 纯净的强电解质在液态时,有的导电,有的不导电 | |
| C. | 同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同 | |
| D. | 在溶液中,导电能力强的电解质为强电解质,导电能力弱的电解质是弱电解质 |
 (1)NO2-的定性检验:在酸性介质中,NO2-和Fe2+反应产生棕色的[Fe(NO)]2+(N为+2价),反应的离子方程式为2Fe2++NO2-+2H+═Fe3++[Fe(NO)]2++H2O.
(1)NO2-的定性检验:在酸性介质中,NO2-和Fe2+反应产生棕色的[Fe(NO)]2+(N为+2价),反应的离子方程式为2Fe2++NO2-+2H+═Fe3++[Fe(NO)]2++H2O.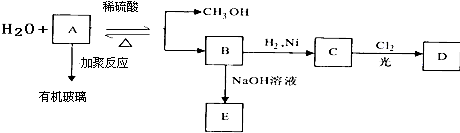
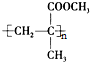 .
. ;
;