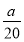题目内容
(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是 。
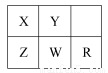
(2)已知某粒子的结构示意图为: ,试回答:
,试回答:
①当x-y=10时,该粒子为 (填“原子”“阳离子”或“阴离子”)。
②当y=8时,粒子可能为(填名称) 、 、 、 、 。
(1)
(2)①原子 ②氩原子;氯离子;硫离子;钾离子;钙离子 ③Al(OH)3+3H+=Al3++3H2O
③写出y=3与y=7的元素最高价氧化物对应水化物之间发生反应的离子方程式 。
【解析】(1)设该元素原子的核电荷数=质子数=a,电子层数为x,最外层电子数为y,依题意:a=5x,a=3y,则5x=3y。因原子的最外层电子数不超过8,即y为1~8的正整数,故仅当y=5,x=3时合理,该元素的核电荷数为15。(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为原子;②当y=8时,应为有18个电子的粒子,所以可能为氩原子、氯离子、硫离子、钾离子、钙离子;③y=3时为铝原子、y=7时为氯原子,其最高价氧化物对应的水化物分别为氢氧化铝和高氯酸,反应的离子方程式为Al(OH)3+3H+=Al3++3H2O。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目