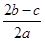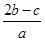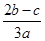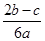题目内容
取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为 ( )
| A.3.2mol/L | B.2.8mol/L | C.1.8mol/L | D.缺数据无法计算 |
A
解析试题分析:设有xmol的铜、ymol的氧化亚铜、zmol的氧化铜,硝酸的物质的量浓度为M,得:
y+z=6.4/16
2(x+2y+z)+4.48/22.4=0.5M
x+y=4.48/22.4*1.5
解得M=3.2
考点:氧化还原反应。

练习册系列答案
相关题目
NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A.1mol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA |
| B.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA |
| C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA |
| D.t℃时,MgCO3的KSP=4×10-6,,则饱和溶液中含Mg2+数目为2×10-3NA |
在标况下,将O2与NO2按1:4的体积比充满于一真空干燥烧瓶中,然后将烧瓶倒置于水中,瓶中液面逐渐上升后,至几乎完全充满烧瓶,最终烧瓶内溶液的物质的量浓度最接近于
| A.0.026mol/L | B.0.030mol/L | C.0.036mol/L | D.0.045mol/L |
NA表示阿伏加德罗常数。下列说法正确的是( )
| A.0.1mol Na2O2中含有的阴离子数目为0.2NA |
| B.标准状况下,2.24 L CHCl3的分子数为0.1NA |
| C.1 L 0.1 mol·L-1 Al2(SO4)3溶液中Al3+的数目为0.2NA |
| D.9.2 g NO2和N2O4的混合气体中含有的氮原子数为0.2NA |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.46g乙醇中含有的化学键数为7NA |
| B.1mol氯气和足量NaOH溶液反应转移电子数为2NA |
| C.1molOH-和1mol–OH(羟基)中含有的质子数均为9NA |
| D.10L0.1mol·L-1的Na2CO3溶液中,Na+、CO32-总数为3NA |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温下,10LpH=13的NaOH溶液中含有的OH-离子数为NA |
| C.标准状况下,11.2L己烷中含有分子的数目为0.5NA |
| D.100mL0.1mol·L-1的FeCl3溶液中含有Fe3+的个数为0.01 NA |
用密度1.19g/cm3质量分数为37%的浓盐酸配制稀盐酸:①用浓盐酸与等体积的水混合后所得稀盐酸的质量分数为a%②用浓盐酸与等质量的水混合后所得的稀盐酸的质量分数为b%,那么a与b的关系正确的是
| A.a>b | B.a="b" | C.a<b | D.无法确定 |
设阿伏伽德罗常数的值为NA,下列说法正确的是:
| A.0.5mol的NaHSO4固体中含有的阴离子总数为NA |
| B.0.1mol/L FeCl3的溶液中,含Cl-数目为0.3 NA |
| C.标准状况下22.4LNO2气体与水完全反应时,转移电子数目为NA |
| D.常温常压下,23gNO2和N2O4的混合气体中总原子数目为1.5 NA |
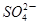 完全沉淀;向另一等份加入足量NaOH固体并加热可得到c mol NH3,则原溶液中Fe3+的物质的量浓度为( )mol·L-1
完全沉淀;向另一等份加入足量NaOH固体并加热可得到c mol NH3,则原溶液中Fe3+的物质的量浓度为( )mol·L-1